Aktiviti 3.18:
Tujuan: Menulis persamaan kimia yang seimbang.
Bahan: Serbuk kuprum(II) karbonat, air kapur, asid hidroklorik pekat, larutan ammonia pekat, larutan plumbum(II) nitrat dan larutan kalium iodida
Radas: Tabung uji, salur penghantar dan penyumbat getah, pemegang tabung uji, penunu Bunsen, silinder penyukat 10 cm3, spatula, penyumbat tabung uji dan salur kaca
Prosedur:
(A) Pemanasan kuprum(II) karbonat
1. Isikan satu spatula serbuk kuprum(II) karbonat ke dalam tabung uji. Perhatikan warna serbuk itu.
2. Sediakan susunan radas seperti dalam Rajah 3.18.
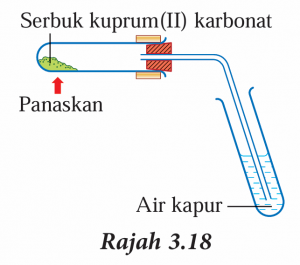
3. Panaskan kuprum(II) karbonat dan alirkan gas yang terhasil ke dalam air kapur. Perhatikan perubahan yang berlaku di dalam kedua-dua tabung uji.
4. Apabila tindak balas telah selesai, alihkan tabung uji berisi air kapur. Kemudian, hentikan pemanasan.
5. Rekod pemerhatian anda.
(B) Pembentukan ammonium klorida
1. Dengan menggunakan salur kaca, titiskan 3 atau 4 titis asid hidroklorik pekat ke dalam sebuah tabung uji. Tutupkan mulut tabung uji dengan penyumbat dan biarkan selama beberapa minit.
2. Ulang langkah 1 dengan menitiskan larutan ammonia pekat ke dalam tabung uji lain.
3. Alihkan penyumbat pada kedua-dua tabung uji. Dengan cepat, dekatkan mulut tabung uji seperti dalam Rajah 3.19.
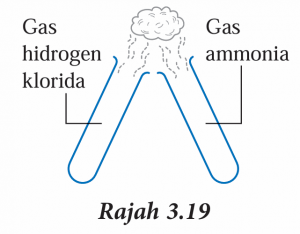
4. Perhatikan perubahan yang berlaku dan rekod pemerhatian.
(C) Pemendakan plumbum(II) iodida
1. Tuangkan 2.0 cm3 larutan plumbum(II) nitrat ke dalam tabung uji.
2. Tuangkan 2.0 cm3 larutan kalium iodida ke dalam tabung uji lain.
3. Tuangkan larutan kalium iodida ke dalam larutan plumbum(II) nitrat seperti dalam Rajah 3.20. Goncangkan campuran itu.
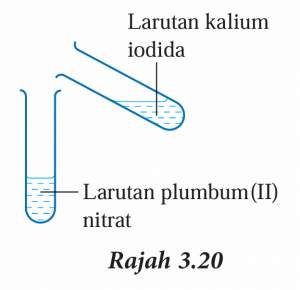
4. Perhatikan perubahan yang berlaku dan rekod pemerhatian.
Perbincangan:
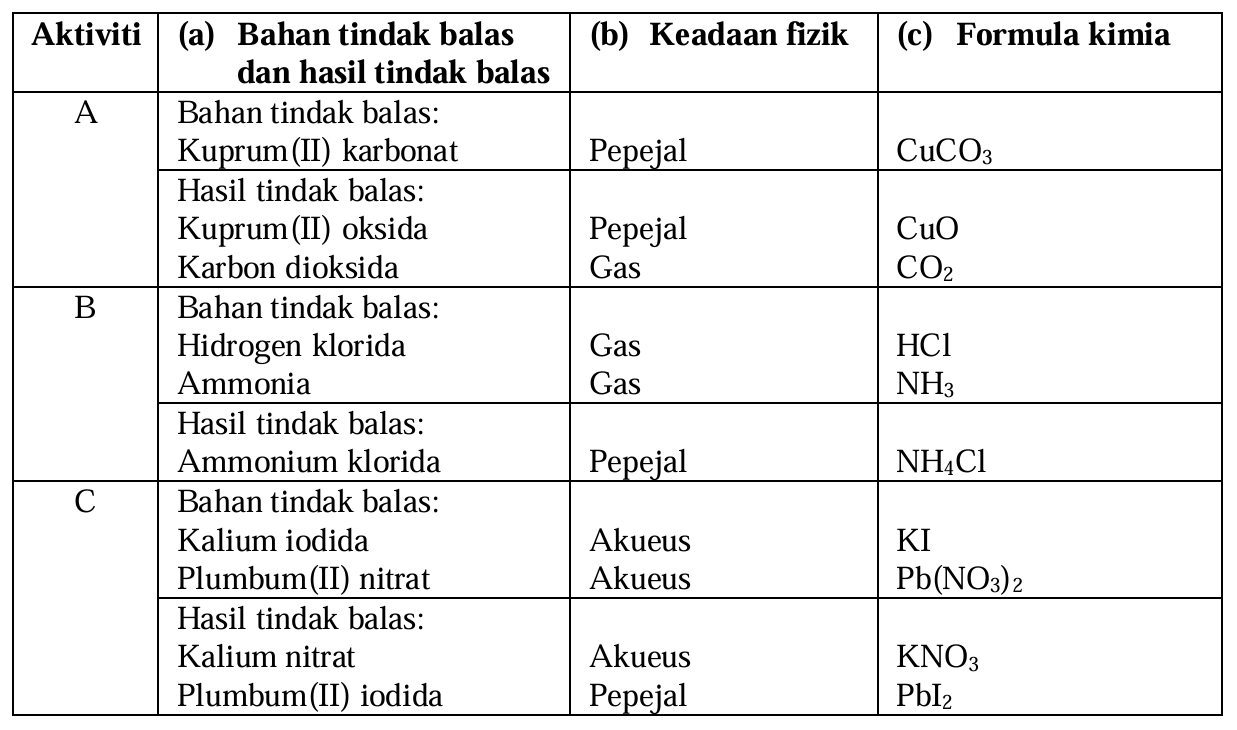
1. Bagi setiap tindak balas A, B, dan C, nyatakan:
(a) bahan tindak balas dan hasil tindak balas.
(b) keadaan fizik setiap bahan tindak balas dan hasil tindak balas.
(c) formula kimia setiap bahan tindak balas dan hasil tindak balas.
2. Tulis persamaan kimia yang seimbang bagi setiap tindak balas tersebut.
Jawapan:
Perbincangan:
1.
2. Tindak balas A
CuCO3(p) → CuO(p) + CO2(g)
Tindak balas B
HCl(g) + NH3(g) → NH4Cl(p)
Tindak balas C
2KI(ak) + Pb(NO3)2(ak) → 2KNO3(ak) + PbI2(p)
Tujuan: Menulis persamaan kimia yang seimbang.
Bahan: Serbuk kuprum(II) karbonat, air kapur, asid hidroklorik pekat, larutan ammonia pekat, larutan plumbum(II) nitrat dan larutan kalium iodida
Radas: Tabung uji, salur penghantar dan penyumbat getah, pemegang tabung uji, penunu Bunsen, silinder penyukat 10 cm3, spatula, penyumbat tabung uji dan salur kaca
Prosedur:
(A) Pemanasan kuprum(II) karbonat
1. Isikan satu spatula serbuk kuprum(II) karbonat ke dalam tabung uji. Perhatikan warna serbuk itu.
2. Sediakan susunan radas seperti dalam Rajah 3.18.

3. Panaskan kuprum(II) karbonat dan alirkan gas yang terhasil ke dalam air kapur. Perhatikan perubahan yang berlaku di dalam kedua-dua tabung uji.
4. Apabila tindak balas telah selesai, alihkan tabung uji berisi air kapur. Kemudian, hentikan pemanasan.
5. Rekod pemerhatian anda.
(B) Pembentukan ammonium klorida
1. Dengan menggunakan salur kaca, titiskan 3 atau 4 titis asid hidroklorik pekat ke dalam sebuah tabung uji. Tutupkan mulut tabung uji dengan penyumbat dan biarkan selama beberapa minit.
2. Ulang langkah 1 dengan menitiskan larutan ammonia pekat ke dalam tabung uji lain.
3. Alihkan penyumbat pada kedua-dua tabung uji. Dengan cepat, dekatkan mulut tabung uji seperti dalam Rajah 3.19.

4. Perhatikan perubahan yang berlaku dan rekod pemerhatian.
(C) Pemendakan plumbum(II) iodida
1. Tuangkan 2.0 cm3 larutan plumbum(II) nitrat ke dalam tabung uji.
2. Tuangkan 2.0 cm3 larutan kalium iodida ke dalam tabung uji lain.
3. Tuangkan larutan kalium iodida ke dalam larutan plumbum(II) nitrat seperti dalam Rajah 3.20. Goncangkan campuran itu.

4. Perhatikan perubahan yang berlaku dan rekod pemerhatian.
Perbincangan:
1. Bagi setiap tindak balas A, B, dan C, nyatakan:
(a) bahan tindak balas dan hasil tindak balas.
(b) keadaan fizik setiap bahan tindak balas dan hasil tindak balas.
(c) formula kimia setiap bahan tindak balas dan hasil tindak balas.
2. Tulis persamaan kimia yang seimbang bagi setiap tindak balas tersebut.
Jawapan:
Perbincangan:
1.

2. Tindak balas A
CuCO3(p) → CuO(p) + CO2(g)
Tindak balas B
HCl(g) + NH3(g) → NH4Cl(p)
Tindak balas C
2KI(ak) + Pb(NO3)2(ak) → 2KNO3(ak) + PbI2(p)
