Soalan 1:
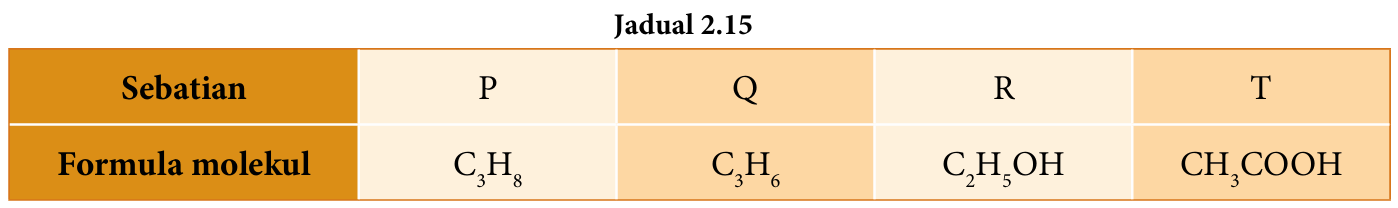
Jadual 2.15 menunjukkan beberapa sebatian karbon dan formula molekul masing-masing.
(a)(i) Bandingkan dan beza kejelagaan nyalaan sebatian P dan sebatian Q apabila terbakar dalam oksigen yang berlebihan. Terangkan jawapan anda.
[Jisim atom relatif: C = 12, H = 1]
(ii) Jadual 2.16 menunjukkan keputusan eksperimen apabila sebatian P dan sebatian Q digoncang di dalam air bromin di dalam tabung uji.
 Berdasarkan Jadual 2.16, terangkan perbezaan dalam pemerhatian.
Berdasarkan Jadual 2.16, terangkan perbezaan dalam pemerhatian.
(b) 2.3 g sebatian R terbakar dengan lengkap dalam oksigen berlebihan untuk menghasilkan gas karbon dioksida dan air. Tuliskan persamaan kimia bagi tindak balas tersebut dan tentukan isipadu gas karbon dioksida yang terhasil. [Jisim molar R = 46 g mol−1, isipadu molar gas pada keadaan bilik = 24 dm3 mol−1]
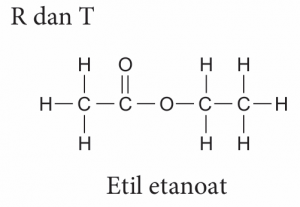
(c) Nyatakan dua sebatian daripada Jadual 2.15 yang bertindak balas untuk menghasilkan ester. Namakan dan lukiskan formula struktur bagi ester yang terbentuk.
(d) Asid X digunakan sebagai mangkin semasa tindak balas pengesteran. Apabila asid X yang pekat tertumpah ke atas lantai marmar maka gelembung gas akan terhasil. Namakan asid X dan tuliskan persamaan kimia bagi tindak balas tersebut.
Jawapan:
(a)(i) – Q terbakar dengan lebih jelaga dibandingkan dengan P
– Peratus jisim karbon dalam molekul P dan Q:
$$ \begin{aligned} &\% C \text { dalam } P=\frac{3(12)}{3(12)+8(1)} \times 100 \%=81.8 \%\\ &\% C \text { dalam } Q=\frac{3(12)}{3(12)+6(1)} \times 100 \%=85.7 \% \end{aligned} $$
– Peratus jisim karbon dalam molekul Q lebih tinggi. Oleh itu Q terbakar lebih berjelaga berbanding P
(a)(ii) – P adalah hidrokarbon tepu yang hanya mempunyai ikatan tunggal antara atom karbon. Tindak balas penambahan tidak berlaku antara sebatian P dengan air bromin.
– Q adalah hidrokarbon tak tepu yang mempunyai ikatan ganda dua antara atom karbon. Tindak balas penambahan berlaku antara molekul Q dengan air bromin:
C3H6 + Br2 → C3H6Br2
(b)
$$ \begin{aligned} &\mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}+3 \mathrm{O}_2 \rightarrow 4 \mathrm{CO}_2+3 \mathrm{H}_2 \mathrm{O}\\ &\text { Bil mol } \mathrm{R}=\frac{2.3 \mathrm{~g}}{46 \mathrm{~g} \mathrm{~mol}^{-1}}=0.05 \mathrm{~mol} \end{aligned} $$
$$ \begin{aligned} & \text { Daripada persamaan: } \quad 1 \mathrm{~mol} \mathrm{C}_2 \mathrm{H}_5 \mathrm{OH} \mathrm{:} 2 \mathrm{~mol} \mathrm{CO}_2 \\ & \quad 0.05 \mathrm{~mol} \mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}: 0.10 \mathrm{~mol} \mathrm{CO}_2 \\ & \begin{aligned} \text { Isi padu } \mathrm{CO}_2= & 0.10 \mathrm{~mol} \times 24 \mathrm{dm}^3 \mathrm{~mol}^{-1} \\ = & 2.4 \mathrm{dm}^3 \end{aligned} \end{aligned} $$
(c)
(d) Asid X adalah asid sulfurik pekat
Persamaan kimia:
2H2SO4 + CaCO3 → CaSO4 + H2O + CO2
Jadual 2.15 menunjukkan beberapa sebatian karbon dan formula molekul masing-masing.

(a)(i) Bandingkan dan beza kejelagaan nyalaan sebatian P dan sebatian Q apabila terbakar dalam oksigen yang berlebihan. Terangkan jawapan anda.
[Jisim atom relatif: C = 12, H = 1]
(ii) Jadual 2.16 menunjukkan keputusan eksperimen apabila sebatian P dan sebatian Q digoncang di dalam air bromin di dalam tabung uji.
 Berdasarkan Jadual 2.16, terangkan perbezaan dalam pemerhatian.
Berdasarkan Jadual 2.16, terangkan perbezaan dalam pemerhatian.(b) 2.3 g sebatian R terbakar dengan lengkap dalam oksigen berlebihan untuk menghasilkan gas karbon dioksida dan air. Tuliskan persamaan kimia bagi tindak balas tersebut dan tentukan isipadu gas karbon dioksida yang terhasil. [Jisim molar R = 46 g mol−1, isipadu molar gas pada keadaan bilik = 24 dm3 mol−1]
(c) Nyatakan dua sebatian daripada Jadual 2.15 yang bertindak balas untuk menghasilkan ester. Namakan dan lukiskan formula struktur bagi ester yang terbentuk.
(d) Asid X digunakan sebagai mangkin semasa tindak balas pengesteran. Apabila asid X yang pekat tertumpah ke atas lantai marmar maka gelembung gas akan terhasil. Namakan asid X dan tuliskan persamaan kimia bagi tindak balas tersebut.
Jawapan:
(a)(i) – Q terbakar dengan lebih jelaga dibandingkan dengan P
– Peratus jisim karbon dalam molekul P dan Q:
$$ \begin{aligned} &\% C \text { dalam } P=\frac{3(12)}{3(12)+8(1)} \times 100 \%=81.8 \%\\ &\% C \text { dalam } Q=\frac{3(12)}{3(12)+6(1)} \times 100 \%=85.7 \% \end{aligned} $$
– Peratus jisim karbon dalam molekul Q lebih tinggi. Oleh itu Q terbakar lebih berjelaga berbanding P
(a)(ii) – P adalah hidrokarbon tepu yang hanya mempunyai ikatan tunggal antara atom karbon. Tindak balas penambahan tidak berlaku antara sebatian P dengan air bromin.
– Q adalah hidrokarbon tak tepu yang mempunyai ikatan ganda dua antara atom karbon. Tindak balas penambahan berlaku antara molekul Q dengan air bromin:
C3H6 + Br2 → C3H6Br2
(b)
$$ \begin{aligned} &\mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}+3 \mathrm{O}_2 \rightarrow 4 \mathrm{CO}_2+3 \mathrm{H}_2 \mathrm{O}\\ &\text { Bil mol } \mathrm{R}=\frac{2.3 \mathrm{~g}}{46 \mathrm{~g} \mathrm{~mol}^{-1}}=0.05 \mathrm{~mol} \end{aligned} $$
$$ \begin{aligned} & \text { Daripada persamaan: } \quad 1 \mathrm{~mol} \mathrm{C}_2 \mathrm{H}_5 \mathrm{OH} \mathrm{:} 2 \mathrm{~mol} \mathrm{CO}_2 \\ & \quad 0.05 \mathrm{~mol} \mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}: 0.10 \mathrm{~mol} \mathrm{CO}_2 \\ & \begin{aligned} \text { Isi padu } \mathrm{CO}_2= & 0.10 \mathrm{~mol} \times 24 \mathrm{dm}^3 \mathrm{~mol}^{-1} \\ = & 2.4 \mathrm{dm}^3 \end{aligned} \end{aligned} $$
(c)

(d) Asid X adalah asid sulfurik pekat
Persamaan kimia:
2H2SO4 + CaCO3 → CaSO4 + H2O + CO2
