Soalan:
6. Rajah 2 menunjukkan respirasi aerobik di dalam sel badan kita untuk menghasilkan tenaga daripada glukosa, C6H12O6.
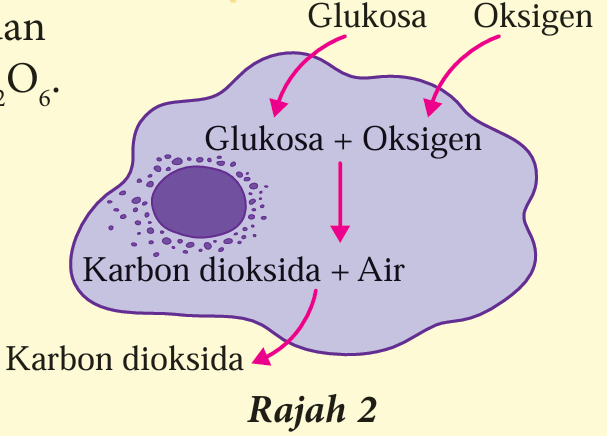
Tulis persamaan kimia yang seimbang bagi proses respirasi aerobik.
7. Ferum(II) sulfat heptahidrat, FeSO4 .7H2O sering digunakan untuk merawat pesakit anemia akibat kekurangan mineral besi.
(a) Apakah jisim molar bagi ferum(II) sulfat heptahidrat?
(b) Hitungkan peratus besi di dalam ferum(II) sulfat heptahidrat.
8. Rajah 3 menunjukkan langkah-langkah penimbangan dalam penentuan formula empirik oksida bagi logam Y.
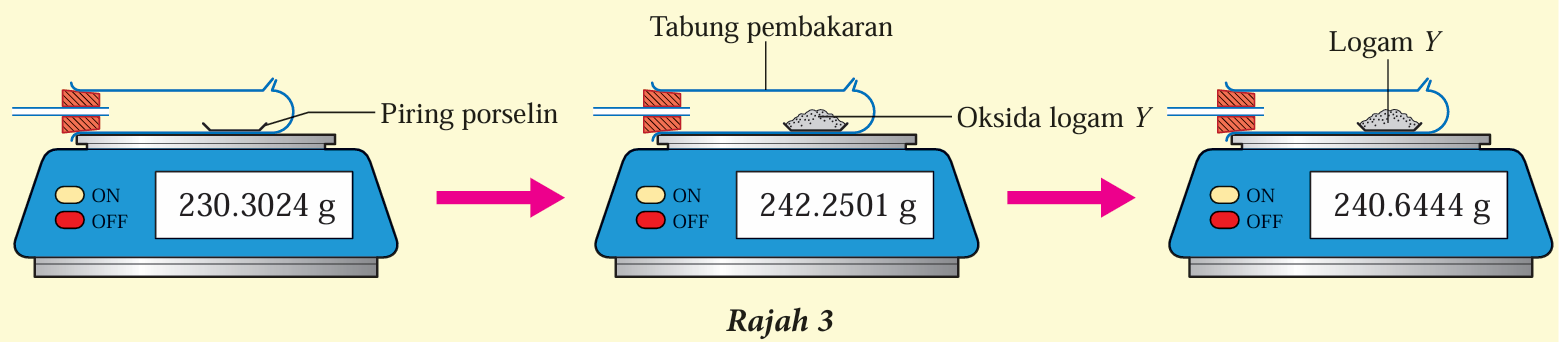
Tentukan formula empirik oksida bagi logam Y. [Jisim atom relatif: O = 16, Y = 207]
9. P, Q, dan R merupakan tiga sampel bahan kimia.
P – 0.2 mol kalsium klorida
Q – 12 dm3 gas nitrogen monoksida pada keadaan bilik
R – 2.408 × 1023 molekul karbon dioksida
Susun ketiga-tiga sampel itu menurut tertib jisim yang menaik.
10. Pada pendapat anda, antara formula empirik atau formula molekul, formula yang manakah lebih sesuai digunakan untuk menulis persamaan kimia? Berikan alasan anda.
Jawapan:
6. C6H12O6(p) + 6O2(g) → 6CO2(g) + 6H2O(ce)
7. (a) 278 g mol-1
(b) 20.14%
8. YO2
9. Q, R, P
10. Formula molekul lebih sesuai digunakan dalam persamaan kerana formula molekul menunjukkan bilangan sebenar setiap jenis atom di dalam molekul sebatian. Oleh yang demikian, stoikiometri persamaan yang menggunakan formula molekul dapat memberikan nisbah bilangan mol sebenar bahan-bahan yang terlibat agar dapat digunakan untuk menyelesaikan pelbagai masalah numerikal tentang tindak balas.
6. Rajah 2 menunjukkan respirasi aerobik di dalam sel badan kita untuk menghasilkan tenaga daripada glukosa, C6H12O6.

Tulis persamaan kimia yang seimbang bagi proses respirasi aerobik.
7. Ferum(II) sulfat heptahidrat, FeSO4 .7H2O sering digunakan untuk merawat pesakit anemia akibat kekurangan mineral besi.
(a) Apakah jisim molar bagi ferum(II) sulfat heptahidrat?
(b) Hitungkan peratus besi di dalam ferum(II) sulfat heptahidrat.
8. Rajah 3 menunjukkan langkah-langkah penimbangan dalam penentuan formula empirik oksida bagi logam Y.

Tentukan formula empirik oksida bagi logam Y. [Jisim atom relatif: O = 16, Y = 207]
9. P, Q, dan R merupakan tiga sampel bahan kimia.
P – 0.2 mol kalsium klorida
Q – 12 dm3 gas nitrogen monoksida pada keadaan bilik
R – 2.408 × 1023 molekul karbon dioksida
Susun ketiga-tiga sampel itu menurut tertib jisim yang menaik.
10. Pada pendapat anda, antara formula empirik atau formula molekul, formula yang manakah lebih sesuai digunakan untuk menulis persamaan kimia? Berikan alasan anda.
Jawapan:
6. C6H12O6(p) + 6O2(g) → 6CO2(g) + 6H2O(ce)
7. (a) 278 g mol-1
(b) 20.14%
8. YO2
9. Q, R, P
10. Formula molekul lebih sesuai digunakan dalam persamaan kerana formula molekul menunjukkan bilangan sebenar setiap jenis atom di dalam molekul sebatian. Oleh yang demikian, stoikiometri persamaan yang menggunakan formula molekul dapat memberikan nisbah bilangan mol sebenar bahan-bahan yang terlibat agar dapat digunakan untuk menyelesaikan pelbagai masalah numerikal tentang tindak balas.
