Eksperimen 4.1:
Tujuan: Mengkaji sifat kimia unsur Kumpulan 1.
Pernyataan masalah: Apakah sifat kimia unsur Kumpulan 1 apabila bertindak balas dengan air, oksigen dan klorin?
Bahan: Litium, natrium, kalium, air suling, kertas turas, kertas litmus merah, gas oksigen dan klorin
Radas: Forseps, jubin putih, besen, pisau, sudu balang gas, balang gas dengan penutup, silinder penyukat 10 cm3 dan penunu Bunsen
(A) Tindak balas unsur Kumpulan 1 dengan air (Demonstrasi guru)
Hipotesis: Apabila menuruni Kumpulan 1, tindak balas antara logam alkali dengan air semakin reaktif.
Pemboleh ubah:
(a) dimanipulasikan : Jenis logam alkali
(b) bergerak balas : Kereaktifan logam alkali dengan air
(c) dimalarkan : Saiz logam alkali
Prosedur:
1. Potongkan litium menjadi saiz yang kecil dengan menggunakan pisau dan forseps. Keringkan potongan di atas kertas turas.
2. Masukkan potongan secara perlahan ke dalam besen yang berisi air seperti yang ditunjukkan dalam Rajah 4.7.
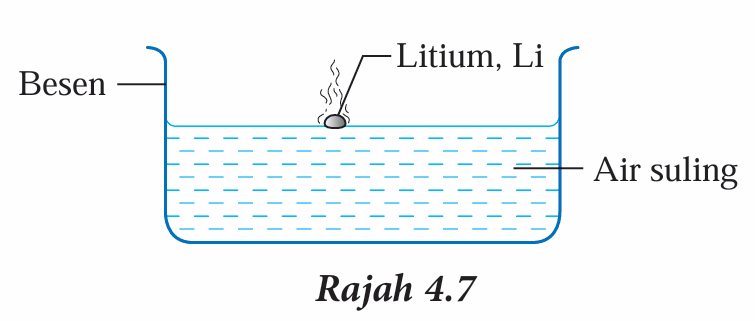
3. Apabila tindak balas selesai, uji larutan dengan menggunakan kertas litmus merah.
4. Catatkan pemerhatian anda.
5. Ulang langkah 1 hingga 4 dengan menggunakan natrium dan kalium.
(B) Tindak balas unsur Kumpulan 1 dengan oksigen
Buat hipotesis dan nyatakan semua pemboleh ubah bagi bahagian B.
Prosedur:
1. Potongkan litium menjadi saiz yang kecil dengan menggunakan pisau dan forseps. Keringkan potongan di atas kertas turas.
2. Letakkan potongan di atas sudu balang gas.
3. Panaskan sehingga potongan mula terbakar dan kemudian masukkan sudu dengan cepat ke dalam balang gas yang berisi gas oksigen seperti yang ditunjukkan dalam Rajah 4.8.
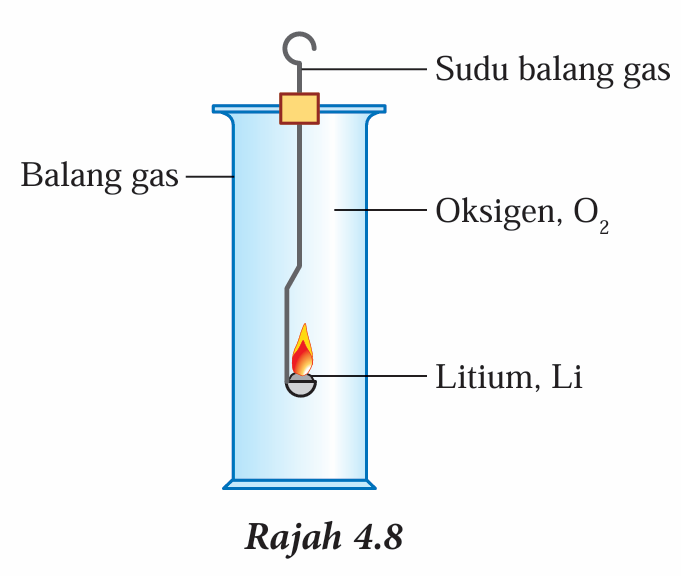
4. Apabila tindak balas selesai, tambahkan 10.0 cm3 air ke dalam balang gas dan goncangkan.
5. Uji larutan dengan menggunakan kertas litmus merah.
6. Catatkan pemerhatian anda.
7. Ulang langkah 1 hingga 6 dengan menggunakan natrium dan kalium.
(C) Tindak balas unsur Kumpulan 1 dengan klorin
Buat hipotesis dan nyatakan semua pemboleh ubah bagi bahagian C.
Prosedur:
1. Potongkan litium menjadi saiz yang kecil dengan menggunakan pisau dan forseps. Keringkan potongan di atas kertas turas.
2. Letakkan potongan di atas sudu balang gas.
3. Panaskan sehingga potongan mula terbakar dan kemudian masukkan sudu dengan cepat ke dalam balang gas yang berisi gas klorin seperti yang ditunjukkan dalam Rajah 4.8.
4. Catatkan pemerhatian anda.
5. Ulang langkah 1 hingga 4 dengan menggunakan natrium dan kalium.
Keputusan:

Kesimpulan:
Adakah hipotesis yang dibuat dapat diterima? Apakah kesimpulan eksperimen ini?
Perbincangan:
1. Tulis persamaan kimia bagi litium, natrium, dan kalium dengan:
(a) air
(b) oksigen
(c) klorin
2. Susun kereaktifan logam litium, natrium, dan kalium dengan air, oksigen dan klorin mengikut tertib menaik.
Jawapan:
Perbincangan
1.(a)
2Li(p) + 2H2O(ce) → 2LiOH(ak) + H2(g)
2Na(p) + 2H2O(ce) → 2NaOH(ak) + H2(g)
2K(p) + 2H2O(ce) → 2KOH(ak) + H2(g)
(b)
4Li(p) + O2(g) → 2Li2O(p)
4Na(p) + O2(g) → 2Na2O(p)
4K(p) + O2(g) → 2K2O(p)
(c)
2Li(p) + Cl2(g) → 2LiCl(p)
2Na(p) + Cl2(g) → 2NaCl(p)
2K(p) + Cl2(g) → 2KCl(p)
2. Dengan air, oksigen dan klorin : Li, Na, K
Tujuan: Mengkaji sifat kimia unsur Kumpulan 1.
Pernyataan masalah: Apakah sifat kimia unsur Kumpulan 1 apabila bertindak balas dengan air, oksigen dan klorin?
Bahan: Litium, natrium, kalium, air suling, kertas turas, kertas litmus merah, gas oksigen dan klorin
Radas: Forseps, jubin putih, besen, pisau, sudu balang gas, balang gas dengan penutup, silinder penyukat 10 cm3 dan penunu Bunsen
(A) Tindak balas unsur Kumpulan 1 dengan air (Demonstrasi guru)
Hipotesis: Apabila menuruni Kumpulan 1, tindak balas antara logam alkali dengan air semakin reaktif.
Pemboleh ubah:
(a) dimanipulasikan : Jenis logam alkali
(b) bergerak balas : Kereaktifan logam alkali dengan air
(c) dimalarkan : Saiz logam alkali
Prosedur:
1. Potongkan litium menjadi saiz yang kecil dengan menggunakan pisau dan forseps. Keringkan potongan di atas kertas turas.
2. Masukkan potongan secara perlahan ke dalam besen yang berisi air seperti yang ditunjukkan dalam Rajah 4.7.

3. Apabila tindak balas selesai, uji larutan dengan menggunakan kertas litmus merah.
4. Catatkan pemerhatian anda.
5. Ulang langkah 1 hingga 4 dengan menggunakan natrium dan kalium.
(B) Tindak balas unsur Kumpulan 1 dengan oksigen
Buat hipotesis dan nyatakan semua pemboleh ubah bagi bahagian B.
Prosedur:
1. Potongkan litium menjadi saiz yang kecil dengan menggunakan pisau dan forseps. Keringkan potongan di atas kertas turas.
2. Letakkan potongan di atas sudu balang gas.
3. Panaskan sehingga potongan mula terbakar dan kemudian masukkan sudu dengan cepat ke dalam balang gas yang berisi gas oksigen seperti yang ditunjukkan dalam Rajah 4.8.

4. Apabila tindak balas selesai, tambahkan 10.0 cm3 air ke dalam balang gas dan goncangkan.
5. Uji larutan dengan menggunakan kertas litmus merah.
6. Catatkan pemerhatian anda.
7. Ulang langkah 1 hingga 6 dengan menggunakan natrium dan kalium.
(C) Tindak balas unsur Kumpulan 1 dengan klorin
Buat hipotesis dan nyatakan semua pemboleh ubah bagi bahagian C.
Prosedur:
1. Potongkan litium menjadi saiz yang kecil dengan menggunakan pisau dan forseps. Keringkan potongan di atas kertas turas.
2. Letakkan potongan di atas sudu balang gas.
3. Panaskan sehingga potongan mula terbakar dan kemudian masukkan sudu dengan cepat ke dalam balang gas yang berisi gas klorin seperti yang ditunjukkan dalam Rajah 4.8.
4. Catatkan pemerhatian anda.
5. Ulang langkah 1 hingga 4 dengan menggunakan natrium dan kalium.
Keputusan:

Kesimpulan:
Adakah hipotesis yang dibuat dapat diterima? Apakah kesimpulan eksperimen ini?
Perbincangan:
1. Tulis persamaan kimia bagi litium, natrium, dan kalium dengan:
(a) air
(b) oksigen
(c) klorin
2. Susun kereaktifan logam litium, natrium, dan kalium dengan air, oksigen dan klorin mengikut tertib menaik.
Jawapan:
Perbincangan
1.(a)
2Li(p) + 2H2O(ce) → 2LiOH(ak) + H2(g)
2Na(p) + 2H2O(ce) → 2NaOH(ak) + H2(g)
2K(p) + 2H2O(ce) → 2KOH(ak) + H2(g)
(b)
4Li(p) + O2(g) → 2Li2O(p)
4Na(p) + O2(g) → 2Na2O(p)
4K(p) + O2(g) → 2K2O(p)
(c)
2Li(p) + Cl2(g) → 2LiCl(p)
2Na(p) + Cl2(g) → 2NaCl(p)
2K(p) + Cl2(g) → 2KCl(p)
2. Dengan air, oksigen dan klorin : Li, Na, K
