Aktiviti 3A:
Seorang pelajar telah menjalankan satu eksperimen untuk menentukan haba penyesaran bagi tindak balas antara kuprum, Cu dengan larutan argentum nitrat, AgNO3. Dalam eksperimen ini, serbuk kuprum, Cu berlebihan ditambah kepada 100 cm3 larutan argentum nitrat, AgNO3 0.5 mol dm−3. Haba penyesaran dalam eksperimen itu ialah – 105 kJ mol−1.
[Muatan haba tentu larutan, c = 4.2 J g−1 °C−1 ; ketumpatan larutan = 1 g cm−3]
(a) Tuliskan persamaan termokimia bagi tindak balas ini.
(b) Hitungkan haba yang dibebaskan dalam eksperimen ini.
(c) Hitungkan perubahan suhu.
(d) Lukiskan gambar rajah aras tenaga bagi tindak balas ini.
(e) Eksperimen ini diulangi dengan menggunakan 100 cm3 larutan argentum nitrat, AgNO3 1.0 mol dm−3 dan serbuk kuprum, Cu berlebihan. Hitungkan perubahan suhu dalam eksperimen ini. Terangkan sebab perubahan suhu ini berbeza daripada yang berlaku di (c).
Jawapan:
(a)
$$ \mathrm{Cu}+2 \mathrm{AgNO}_3 \rightarrow 2 \mathrm{Ag}+\mathrm{Cu}\left(\mathrm{NO}_3\right)_2 \quad \Delta \mathrm{H}=-105 \mathrm{~kJ} \mathrm{~mol}^{-1} $$
(b) Bilangan mol ion argentum
$$ =0.5 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{100}{1000} \mathrm{dm}^3=0.05 \mathrm{~mol} $$
Daripada persamaan termokimia, 1 mol argentum disesarkan membebaskan 105 kJ haba
Maka 0.05 mol argentum disesarkan membebaskan 0.05 mol × 105 kJ mol−1 = 5.25 kJ haba
(c) $$ \begin{aligned} & \mathrm{Q}=\mathrm{mc} \theta \quad \text { maka, } \theta=\frac{\mathrm{Q}}{\mathrm{mc}} \\ & \theta=\frac{5.25 \times 1000 \mathrm{~J}}{100 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1}}=12.5^{\circ} \mathrm{C} \end{aligned} $$
(d)
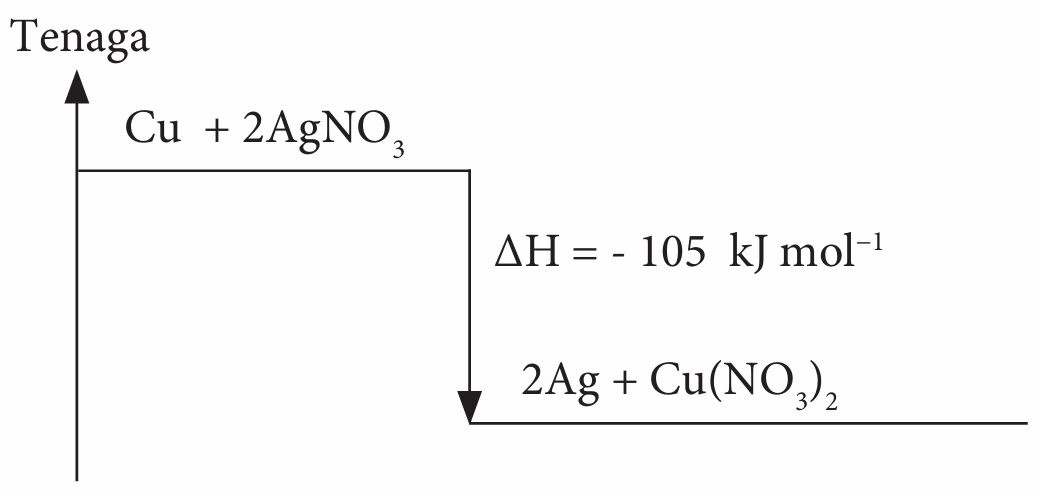
(e) Bilangan mol larutan argentum nitrat
$$ =1.0 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{100}{1000} \mathrm{dm}^3=0.1 \mathrm{~mol} $$
Daripada persamaan termokimia, 1 mol argentum disesarkan membebaskan 105 kJ haba
Maka 0.1 mol argentum disesarkan membebaskan 0.1 mol × 10.5 kJ mol−1 = 10.5 kJ haba
$$ \begin{aligned} & \mathrm{Q}=\mathrm{mc} \theta \quad \text { maka, } \theta=\frac{\mathrm{Q}}{\mathrm{mc}} \\ & \theta=\frac{10.5 \times 1000 \mathrm{~J}}{100 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1}}=25^{\circ} \mathrm{C} \end{aligned} $$
Bilangan mol larutan adalah dua kali ganda, maka perubahan suhu juga dua kali ganda.
Seorang pelajar telah menjalankan satu eksperimen untuk menentukan haba penyesaran bagi tindak balas antara kuprum, Cu dengan larutan argentum nitrat, AgNO3. Dalam eksperimen ini, serbuk kuprum, Cu berlebihan ditambah kepada 100 cm3 larutan argentum nitrat, AgNO3 0.5 mol dm−3. Haba penyesaran dalam eksperimen itu ialah – 105 kJ mol−1.
[Muatan haba tentu larutan, c = 4.2 J g−1 °C−1 ; ketumpatan larutan = 1 g cm−3]
(a) Tuliskan persamaan termokimia bagi tindak balas ini.
(b) Hitungkan haba yang dibebaskan dalam eksperimen ini.
(c) Hitungkan perubahan suhu.
(d) Lukiskan gambar rajah aras tenaga bagi tindak balas ini.
(e) Eksperimen ini diulangi dengan menggunakan 100 cm3 larutan argentum nitrat, AgNO3 1.0 mol dm−3 dan serbuk kuprum, Cu berlebihan. Hitungkan perubahan suhu dalam eksperimen ini. Terangkan sebab perubahan suhu ini berbeza daripada yang berlaku di (c).
Jawapan:
(a)
$$ \mathrm{Cu}+2 \mathrm{AgNO}_3 \rightarrow 2 \mathrm{Ag}+\mathrm{Cu}\left(\mathrm{NO}_3\right)_2 \quad \Delta \mathrm{H}=-105 \mathrm{~kJ} \mathrm{~mol}^{-1} $$
(b) Bilangan mol ion argentum
$$ =0.5 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{100}{1000} \mathrm{dm}^3=0.05 \mathrm{~mol} $$
Daripada persamaan termokimia, 1 mol argentum disesarkan membebaskan 105 kJ haba
Maka 0.05 mol argentum disesarkan membebaskan 0.05 mol × 105 kJ mol−1 = 5.25 kJ haba
(c) $$ \begin{aligned} & \mathrm{Q}=\mathrm{mc} \theta \quad \text { maka, } \theta=\frac{\mathrm{Q}}{\mathrm{mc}} \\ & \theta=\frac{5.25 \times 1000 \mathrm{~J}}{100 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1}}=12.5^{\circ} \mathrm{C} \end{aligned} $$
(d)

(e) Bilangan mol larutan argentum nitrat
$$ =1.0 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{100}{1000} \mathrm{dm}^3=0.1 \mathrm{~mol} $$
Daripada persamaan termokimia, 1 mol argentum disesarkan membebaskan 105 kJ haba
Maka 0.1 mol argentum disesarkan membebaskan 0.1 mol × 10.5 kJ mol−1 = 10.5 kJ haba
$$ \begin{aligned} & \mathrm{Q}=\mathrm{mc} \theta \quad \text { maka, } \theta=\frac{\mathrm{Q}}{\mathrm{mc}} \\ & \theta=\frac{10.5 \times 1000 \mathrm{~J}}{100 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1}}=25^{\circ} \mathrm{C} \end{aligned} $$
Bilangan mol larutan adalah dua kali ganda, maka perubahan suhu juga dua kali ganda.
