Aktiviti 3B:
Apabila 100 cm3 asid hidroklorik cair, HCl 2.0 mol dm−3 ditambahkan ke dalam 100 cm3 larutan natrium hidroksida, NaOH, 2.0 mol dm−3, suhu tindak balas meningkat dari 30.0 °C kepada 43.5 °C. [Muatan haba tentu larutan, c = 4.2 J g−1 °C−1; ketumpatan larutan = 1 g cm−3]
(a) Hitungkan haba peneutralan.
(b) Tuliskan persamaan termokimia.
(c) Lukiskan gambar rajah aras tenaga.
(d) Ramalkan perubahan suhu jika asid hidroklorik, HCl digantikan dengan asid nitrik, HNO3 yang sama isi padu dan kepekatannya. Jelaskan jawapan anda.
Jawapan:
(a) $$ \begin{aligned} & \text { Jisim } \mathrm{m}=(100+100) \mathrm{cm}^3 \times 1 \mathrm{~g} \mathrm{~cm}^{-3}=200 \mathrm{~g} \\ & \text { Perubahan suhu, } \theta=(43.5-30.0)^{\circ} \mathrm{C}=13.5^{\circ} \mathrm{C} \\ & \mathrm{Q}=2000 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1} \times 13.5^{\circ} \mathrm{C}=11340 \mathrm{~J} \end{aligned} $$
Bilangan mol air = Bilangan mol ion hidrogen atau bilangan mol ion hidroksida
$$ =2.0 \mathrm{~mol} \mathrm{dm} \mathrm{dm}^{-3} \times \frac{100}{1000} \mathrm{dm}^3=0.2 \mathrm{~mol} $$
Peneutralan 0.2 mol ion hidrogen oleh 0.2 mol ion hidroksida membebaskan 11340 J haba
Maka peneutralan 1 mol ion hidrogen oleh 1 mol ion hidroksida akan membebaskan
$$ =11340 \mathrm{~J} \times \frac{1 \mathrm{~mol}}{0.02 \mathrm{~mol}}=5670 \mathrm{~J}=56.7 \mathrm{~kJ} $$
Haba peneutralan, ∆H = -56.7 kJ mol−1
(b) $$ \mathrm{HCl}+\mathrm{NaOH} \rightarrow \mathrm{NaCl}+\mathrm{H}_2 \mathrm{O} \quad \Delta \mathrm{H}=-56.7 \mathrm{~kJ} \mathrm{~mol}^{-1} $$
(c)
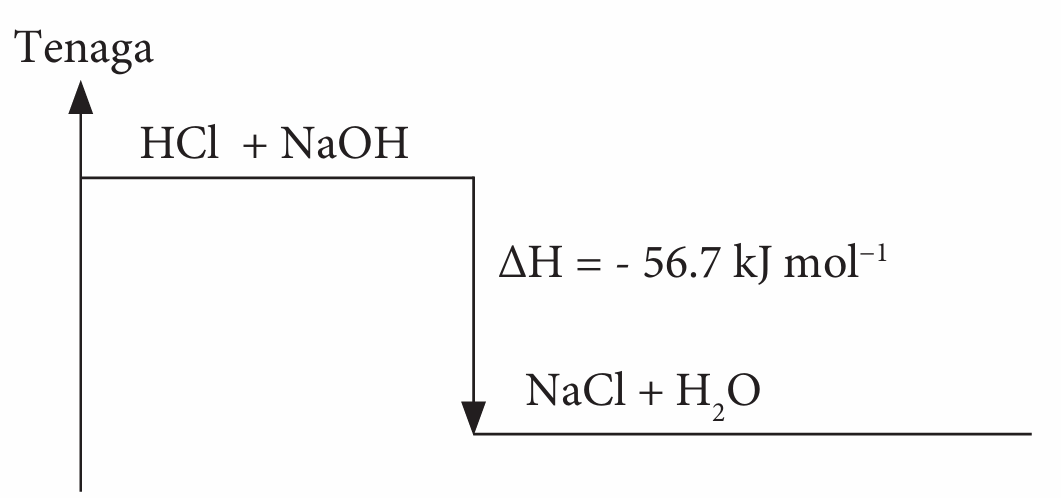
(d) Perubahan suhu adalah sama iaitu 13.5 °C. Asid nitrik ialah asid kuat dan mengion dengan lengkap dalam air.
Apabila 100 cm3 asid hidroklorik cair, HCl 2.0 mol dm−3 ditambahkan ke dalam 100 cm3 larutan natrium hidroksida, NaOH, 2.0 mol dm−3, suhu tindak balas meningkat dari 30.0 °C kepada 43.5 °C. [Muatan haba tentu larutan, c = 4.2 J g−1 °C−1; ketumpatan larutan = 1 g cm−3]
(a) Hitungkan haba peneutralan.
(b) Tuliskan persamaan termokimia.
(c) Lukiskan gambar rajah aras tenaga.
(d) Ramalkan perubahan suhu jika asid hidroklorik, HCl digantikan dengan asid nitrik, HNO3 yang sama isi padu dan kepekatannya. Jelaskan jawapan anda.
Jawapan:
(a) $$ \begin{aligned} & \text { Jisim } \mathrm{m}=(100+100) \mathrm{cm}^3 \times 1 \mathrm{~g} \mathrm{~cm}^{-3}=200 \mathrm{~g} \\ & \text { Perubahan suhu, } \theta=(43.5-30.0)^{\circ} \mathrm{C}=13.5^{\circ} \mathrm{C} \\ & \mathrm{Q}=2000 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1} \times 13.5^{\circ} \mathrm{C}=11340 \mathrm{~J} \end{aligned} $$
Bilangan mol air = Bilangan mol ion hidrogen atau bilangan mol ion hidroksida
$$ =2.0 \mathrm{~mol} \mathrm{dm} \mathrm{dm}^{-3} \times \frac{100}{1000} \mathrm{dm}^3=0.2 \mathrm{~mol} $$
Peneutralan 0.2 mol ion hidrogen oleh 0.2 mol ion hidroksida membebaskan 11340 J haba
Maka peneutralan 1 mol ion hidrogen oleh 1 mol ion hidroksida akan membebaskan
$$ =11340 \mathrm{~J} \times \frac{1 \mathrm{~mol}}{0.02 \mathrm{~mol}}=5670 \mathrm{~J}=56.7 \mathrm{~kJ} $$
Haba peneutralan, ∆H = -56.7 kJ mol−1
(b) $$ \mathrm{HCl}+\mathrm{NaOH} \rightarrow \mathrm{NaCl}+\mathrm{H}_2 \mathrm{O} \quad \Delta \mathrm{H}=-56.7 \mathrm{~kJ} \mathrm{~mol}^{-1} $$
(c)

(d) Perubahan suhu adalah sama iaitu 13.5 °C. Asid nitrik ialah asid kuat dan mengion dengan lengkap dalam air.
