Aktiviti Makmal 3B (Menentukan Haba Pemendakan):
Tujuan : Menentukan haba pemendakan bagi argentum klorida, AgCl dan magnesium karbonat, MgCO3.
Bahan : Larutan argentum nitrat, AgNO3 0.5 mol dm−3, larutan natrium klorida, NaCl 0.5 mol dm−3, larutan magnesium nitrat, Mg(NO3)2 0.5 mol dm−3 dan larutan natrium karbonat, Na2CO3 0.5 mol dm−3.
Radas : Dua buah cawan polistirena dengan penutup, silinder penyukat dan termometer.
Definisi secara operasi – Haba Pemendakan: Apabila larutan natrium klorida, NaCl ditambahkan kepada larutan argentum nitrat, AgNO3 untuk menghasilkan 1 mol mendakan argentum klorida, AgCl bacaan termometer meningkat.
Prosedur:
1. Sukat 25 cm3 larutan argentum nitrat, AgNO3 0.5 mol dm−3 dan tuangkan ke dalam cawan polistirena.
2. Masukkan termometer ke dalam larutan itu dan biarkan selama dua minit.
3. Catatkan suhu larutan.
4. Sukat 25 cm3 larutan natrium klorida, NaCl 0.5 mol dm−3, dan tuangkannya ke dalam cawan polistirena yang lain.
5. Masukkan termometer ke dalam larutan itu dan biarkan selama dua minit. Catatkan suhu larutan.
6. Tuangkan larutan natrium klorida, NaCl dengan cepat dan cermat ke dalam cawan polistirena yang mengandungi larutan argentum nitrat, AgNO3.
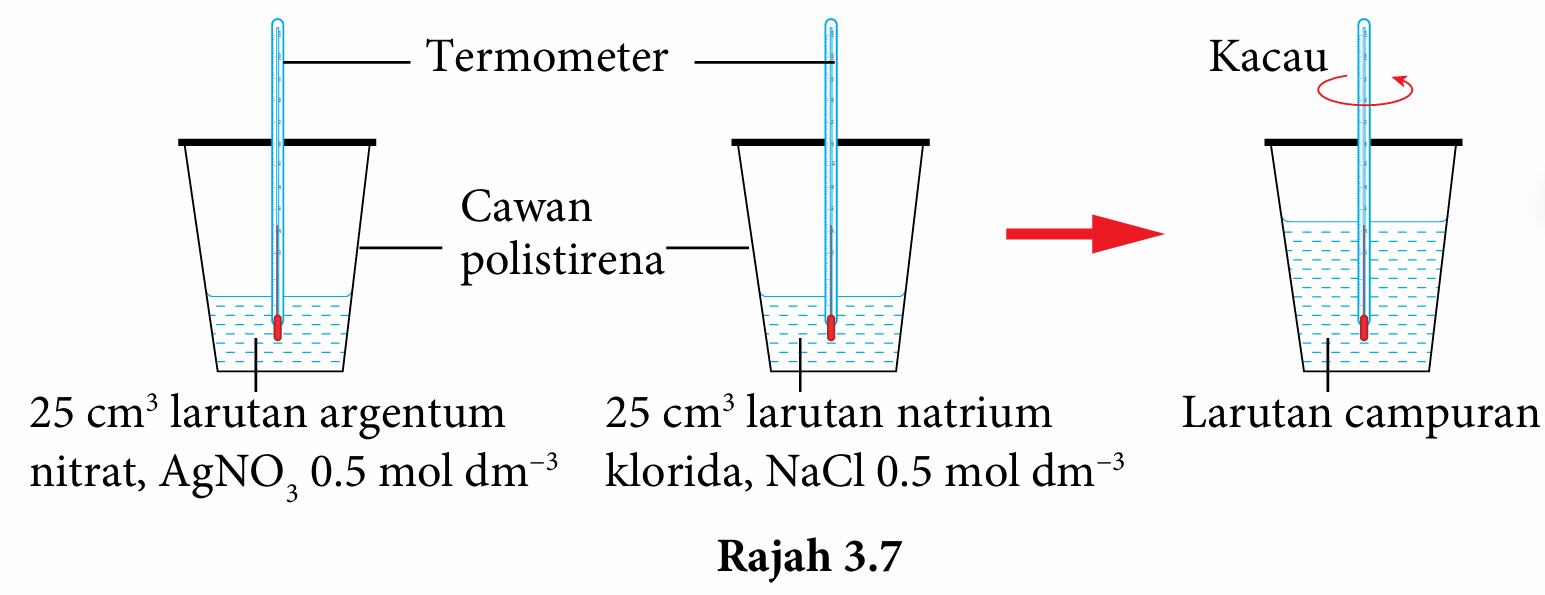
7. Tutup cawan polisterina dengan penutup dan kacaukan campuran dengan termometer seperti yang ditunjukkan pada Rajah 3.7.
8. Catatkan suhu tertinggi campuran.
9. Ulangi langkah 1 hingga 8 dengan menggantikan larutan argentum nitrat, AgNO3 dengan larutan magnesium nitrat, Mg(NO3)2 dan larutan natrium klorida, NaCl dengan larutan natrium karbonat, Na2CO3.
Keputusan:
Bina jadual bersesuaian untuk merekodkan keputusan dan pemerhatian anda.
Perbincangan:
1. Nyatakan jenis tindak balas yang berlaku.
2. Hitungkan haba pemendakan bagi argentum klorida, AgCl dan magnesium karbonat, MgCO3.
[Gunakan rumus perubahan haba, Q = mcθ]
[Diberi: Muatan haba tentu larutan, c = 4.2 J g−1 °C−1; ketumpatan larutan = 1 g cm−3]
3. Tuliskan persamaan termokimia bagi pemendakan argentum klorida, AgCl dan magnesium karbonat, MgCO3.
4. Lukiskan gambar rajah aras tenaga bagi tindak balas pemendakan argentum klorida, AgCl dan magnesium karbonat, MgCO3.
5. Nilai teori haba pemendakan argentum klorida, AgCl ialah -65.5 kJ mol−1. Adakah nilai ini sama dengan nilai yang diperoleh dalam eksperimen ini? Terangkan sebab bagi jawapan anda.
Kesimpulan:
Apakah kesimpulan bagi eksperimen ini?
Jawapan:
Keputusan:
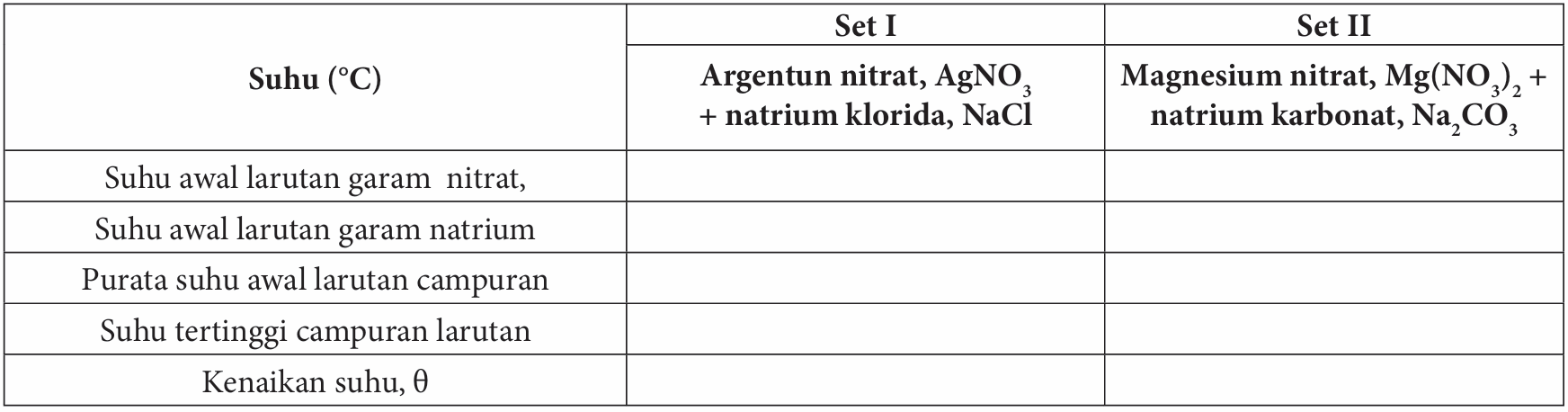
Perbincangan:
1. Tindak balas penguraian ganda dua (tindak balas pemendakan).
2. Langkah-langkah pengiraan:
(a) Haba pemendakan argentum klorida
(i) Hitungkan bilangan mol mendakan argentum klorida, AgCl yang terbentuk
$$ \begin{aligned} \text { Bilangan mol ion argentum, } \mathrm{Ag}^{+} & =\text {bilangan mol larutan argentum nitrat, } \mathrm{AgNO}_3 \\ & =0.5 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{25}{1000} \mathrm{dm}^3=0.0125 \mathrm{~mol} \\ \text { Bilangan mol ion klorida, } \mathrm{Cl}^{-} & =\text {bilangan mol larutan natrium klorida, } \mathrm{NaCl} \\ & =0.5 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{25}{1000} \mathrm{dm}^3=0.0125 \mathrm{~mol} \end{aligned} $$
Persamaan ion : Ag+(ak) + Cl−(ak) → AgCl(p)
Daripada persamaan ion, 1 mol ion argentum, Ag+ bertindak balas dengan 1 mol ion klorida, Cl− menghasilkan 1 mol argentum klorida, AgCl.
Oleh itu 0.0125 mol ion argentum, Ag+ bertindak balas dengan 0.0125 mol ion klorida, Cl− menghasilkan 0.0125 mol argentum klorida, AgCl.
(ii) Hitungkan perubahan haba:
$$ \begin{aligned} &\begin{aligned} \text { Jisim larutan campuran, } \mathrm{m} & =\text { Jumlah isi padu larutan campuran } \text { × } \text { ketumpatan larutan } \\ & =(25+25) \mathrm{cm}^3 \times 1 \mathrm{~g} \mathrm{~cm}^{-3}=200 \mathrm{~g} \end{aligned}\\ &\text { Perubahan suhu larutan campuran, } \theta=\text { Suhu tertinggi }- \text { suhu awal }\\ &\text { Haba yang dibebaskan dalam tindak balas, } \begin{aligned} \mathrm{H} & =\mathrm{mc} \theta \\ & =200 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1} \times \theta \\ & =x \mathrm{~J} \end{aligned} \end{aligned} $$
(iii) Hitungkan perubahan haba untuk pembentukan 1 mol pemendakan:
Pemendakan 0.0125 mol argentum klorida membebaskan x J haba
$$ \begin{aligned} \text { Maka pemendakan } 1 \mathrm{~mol} \text { argentum klorida membebaskan } & =x \mathrm{~J} \times \frac{1 \mathrm{~mol}}{0.0125 \mathrm{~mol}} \\ & =80 x \mathrm{~J} \text { haba } \\ & =0.08 x \mathrm{~kJ} \text { haba } \end{aligned} $$
(iv) Tuliskan haba pemendakan dengan meletakkan tanda negatif bagi tindak balas eksotermik.
Haba pemendakan argentum klorida = – 0.08 x kJ mol−1
Nota: Ikut langkah yang sama untuk haba pemendakan magnesium karbonat
3. Persamaan termokimia bagi pemendakan argentum klorida:
AgNO3 + NaCl → AgCl + NaNO3 ∆H = – 0.08 x kJ mol−1
Persamaan termokimia bagi pemendakan magnesium karbonat:
Mg(NO3)2 + Na2CO3 → MgCO3 + 2NaNO3 ∆H = -(Nilai kiraan) kJ mol−1
4. Gambar rajah aras tenaga bagi haba pemendakan argentum klorida
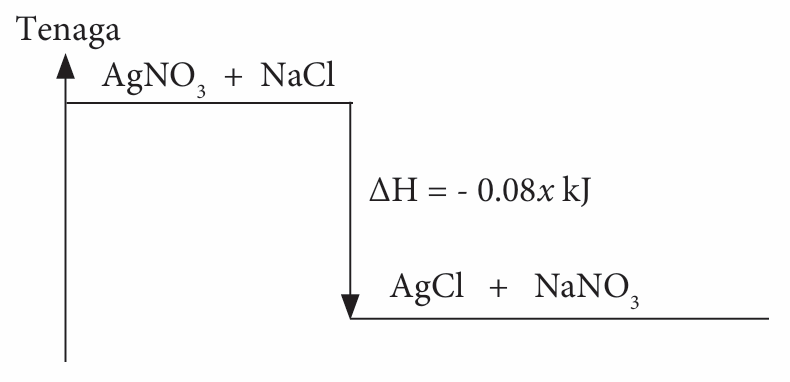
Gambar rajah aras tenaga bagi haba pemendakan magnesium karbonat
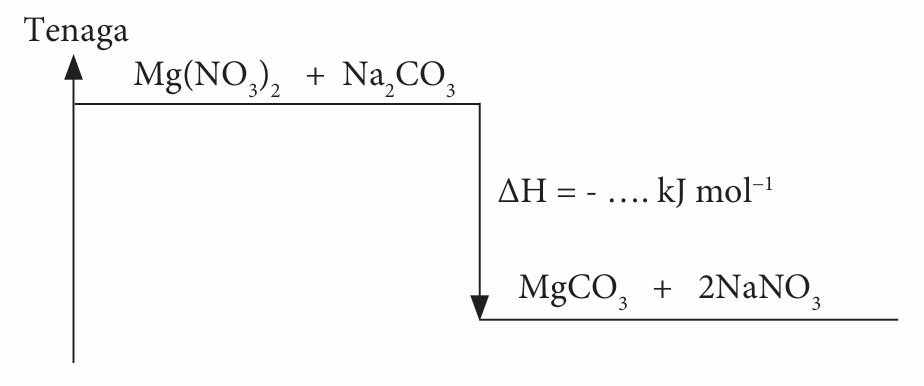
5. Tidak sama.
Perbezaan disebabkan:
(i) Haba terbebas ke persekitaran.
(ii) Cawan polistirena menyerap haba.
Tujuan : Menentukan haba pemendakan bagi argentum klorida, AgCl dan magnesium karbonat, MgCO3.
Bahan : Larutan argentum nitrat, AgNO3 0.5 mol dm−3, larutan natrium klorida, NaCl 0.5 mol dm−3, larutan magnesium nitrat, Mg(NO3)2 0.5 mol dm−3 dan larutan natrium karbonat, Na2CO3 0.5 mol dm−3.
Radas : Dua buah cawan polistirena dengan penutup, silinder penyukat dan termometer.
Definisi secara operasi – Haba Pemendakan: Apabila larutan natrium klorida, NaCl ditambahkan kepada larutan argentum nitrat, AgNO3 untuk menghasilkan 1 mol mendakan argentum klorida, AgCl bacaan termometer meningkat.
Prosedur:
1. Sukat 25 cm3 larutan argentum nitrat, AgNO3 0.5 mol dm−3 dan tuangkan ke dalam cawan polistirena.
2. Masukkan termometer ke dalam larutan itu dan biarkan selama dua minit.
3. Catatkan suhu larutan.
4. Sukat 25 cm3 larutan natrium klorida, NaCl 0.5 mol dm−3, dan tuangkannya ke dalam cawan polistirena yang lain.
5. Masukkan termometer ke dalam larutan itu dan biarkan selama dua minit. Catatkan suhu larutan.
6. Tuangkan larutan natrium klorida, NaCl dengan cepat dan cermat ke dalam cawan polistirena yang mengandungi larutan argentum nitrat, AgNO3.

7. Tutup cawan polisterina dengan penutup dan kacaukan campuran dengan termometer seperti yang ditunjukkan pada Rajah 3.7.
8. Catatkan suhu tertinggi campuran.
9. Ulangi langkah 1 hingga 8 dengan menggantikan larutan argentum nitrat, AgNO3 dengan larutan magnesium nitrat, Mg(NO3)2 dan larutan natrium klorida, NaCl dengan larutan natrium karbonat, Na2CO3.
Keputusan:
Bina jadual bersesuaian untuk merekodkan keputusan dan pemerhatian anda.
Perbincangan:
1. Nyatakan jenis tindak balas yang berlaku.
2. Hitungkan haba pemendakan bagi argentum klorida, AgCl dan magnesium karbonat, MgCO3.
[Gunakan rumus perubahan haba, Q = mcθ]
[Diberi: Muatan haba tentu larutan, c = 4.2 J g−1 °C−1; ketumpatan larutan = 1 g cm−3]
3. Tuliskan persamaan termokimia bagi pemendakan argentum klorida, AgCl dan magnesium karbonat, MgCO3.
4. Lukiskan gambar rajah aras tenaga bagi tindak balas pemendakan argentum klorida, AgCl dan magnesium karbonat, MgCO3.
5. Nilai teori haba pemendakan argentum klorida, AgCl ialah -65.5 kJ mol−1. Adakah nilai ini sama dengan nilai yang diperoleh dalam eksperimen ini? Terangkan sebab bagi jawapan anda.
Kesimpulan:
Apakah kesimpulan bagi eksperimen ini?
Jawapan:
Keputusan:

Perbincangan:
1. Tindak balas penguraian ganda dua (tindak balas pemendakan).
2. Langkah-langkah pengiraan:
(a) Haba pemendakan argentum klorida
(i) Hitungkan bilangan mol mendakan argentum klorida, AgCl yang terbentuk
$$ \begin{aligned} \text { Bilangan mol ion argentum, } \mathrm{Ag}^{+} & =\text {bilangan mol larutan argentum nitrat, } \mathrm{AgNO}_3 \\ & =0.5 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{25}{1000} \mathrm{dm}^3=0.0125 \mathrm{~mol} \\ \text { Bilangan mol ion klorida, } \mathrm{Cl}^{-} & =\text {bilangan mol larutan natrium klorida, } \mathrm{NaCl} \\ & =0.5 \mathrm{~mol} \mathrm{dm}^{-3} \times \frac{25}{1000} \mathrm{dm}^3=0.0125 \mathrm{~mol} \end{aligned} $$
Persamaan ion : Ag+(ak) + Cl−(ak) → AgCl(p)
Daripada persamaan ion, 1 mol ion argentum, Ag+ bertindak balas dengan 1 mol ion klorida, Cl− menghasilkan 1 mol argentum klorida, AgCl.
Oleh itu 0.0125 mol ion argentum, Ag+ bertindak balas dengan 0.0125 mol ion klorida, Cl− menghasilkan 0.0125 mol argentum klorida, AgCl.
(ii) Hitungkan perubahan haba:
$$ \begin{aligned} &\begin{aligned} \text { Jisim larutan campuran, } \mathrm{m} & =\text { Jumlah isi padu larutan campuran } \text { × } \text { ketumpatan larutan } \\ & =(25+25) \mathrm{cm}^3 \times 1 \mathrm{~g} \mathrm{~cm}^{-3}=200 \mathrm{~g} \end{aligned}\\ &\text { Perubahan suhu larutan campuran, } \theta=\text { Suhu tertinggi }- \text { suhu awal }\\ &\text { Haba yang dibebaskan dalam tindak balas, } \begin{aligned} \mathrm{H} & =\mathrm{mc} \theta \\ & =200 \mathrm{~g} \times 4.2 \mathrm{~J} \mathrm{~g}^{-1}{ }^{\circ} \mathrm{C}^{-1} \times \theta \\ & =x \mathrm{~J} \end{aligned} \end{aligned} $$
(iii) Hitungkan perubahan haba untuk pembentukan 1 mol pemendakan:
Pemendakan 0.0125 mol argentum klorida membebaskan x J haba
$$ \begin{aligned} \text { Maka pemendakan } 1 \mathrm{~mol} \text { argentum klorida membebaskan } & =x \mathrm{~J} \times \frac{1 \mathrm{~mol}}{0.0125 \mathrm{~mol}} \\ & =80 x \mathrm{~J} \text { haba } \\ & =0.08 x \mathrm{~kJ} \text { haba } \end{aligned} $$
(iv) Tuliskan haba pemendakan dengan meletakkan tanda negatif bagi tindak balas eksotermik.
Haba pemendakan argentum klorida = – 0.08 x kJ mol−1
Nota: Ikut langkah yang sama untuk haba pemendakan magnesium karbonat
3. Persamaan termokimia bagi pemendakan argentum klorida:
AgNO3 + NaCl → AgCl + NaNO3 ∆H = – 0.08 x kJ mol−1
Persamaan termokimia bagi pemendakan magnesium karbonat:
Mg(NO3)2 + Na2CO3 → MgCO3 + 2NaNO3 ∆H = -(Nilai kiraan) kJ mol−1
4. Gambar rajah aras tenaga bagi haba pemendakan argentum klorida

Gambar rajah aras tenaga bagi haba pemendakan magnesium karbonat

5. Tidak sama.
Perbezaan disebabkan:
(i) Haba terbebas ke persekitaran.
(ii) Cawan polistirena menyerap haba.
