Soalan 1:
Bagaimanakah Moseley menyusun unsur dalam Jadual Berkala Unsur?
Jawapan:
Mengikut pertambahan nombor proton.
Bagaimanakah Moseley menyusun unsur dalam Jadual Berkala Unsur?
Jawapan:
Mengikut pertambahan nombor proton.
Soalan 2:
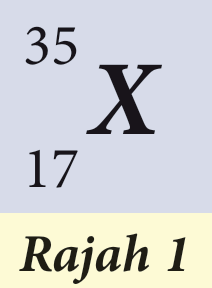
Rajah 1 menunjukkan simbol kimia unsur X.
(a) Apakah kumpulan unsur X dalam Jadual Berkala Unsur?
(b) Apakah kala unsur X dalam Jadual Berkala Unsur?
Jawapan:
(a) Kumpulan 17
(b) Kala 3
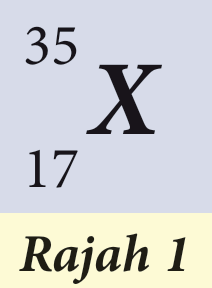
Rajah 1 menunjukkan simbol kimia unsur X.
(a) Apakah kumpulan unsur X dalam Jadual Berkala Unsur?
(b) Apakah kala unsur X dalam Jadual Berkala Unsur?
Jawapan:
(a) Kumpulan 17
(b) Kala 3
Soalan 3:
Seorang pemilik restoran menggunakan lampu elektrik yang berwarna-warni untuk menarik pelanggan datang ke kedainya. Apakah bahan yang sesuai digunakan untuk membuat lampu tersebut?
Jawapan:
Neon
Seorang pemilik restoran menggunakan lampu elektrik yang berwarna-warni untuk menarik pelanggan datang ke kedainya. Apakah bahan yang sesuai digunakan untuk membuat lampu tersebut?
Jawapan:
Neon
Soalan 4:
Nyatakan sifat fizik dan sifat kimia unsur dengan susunan elektron 2.8.8.1.
Jawapan:
Unsur ini merupakan logam yang lembut dan kelabu berkilat. Unsur kumpulan 1 bertindak balas cergas dengan oksigen, air dan gas klorin.
Nyatakan sifat fizik dan sifat kimia unsur dengan susunan elektron 2.8.8.1.
Jawapan:
Unsur ini merupakan logam yang lembut dan kelabu berkilat. Unsur kumpulan 1 bertindak balas cergas dengan oksigen, air dan gas klorin.
Soalan 5:
Nyatakan unsur dalam Kala 3 yang membentuk oksida amfoterik.
Jawapan:
Unsur aluminium
Nyatakan unsur dalam Kala 3 yang membentuk oksida amfoterik.
Jawapan:
Unsur aluminium
Soalan 6:
Rajah 2 menunjukkan beberapa unsur dalam Jadual Berkala Unsur yang diwakili dengan huruf X dan Y.
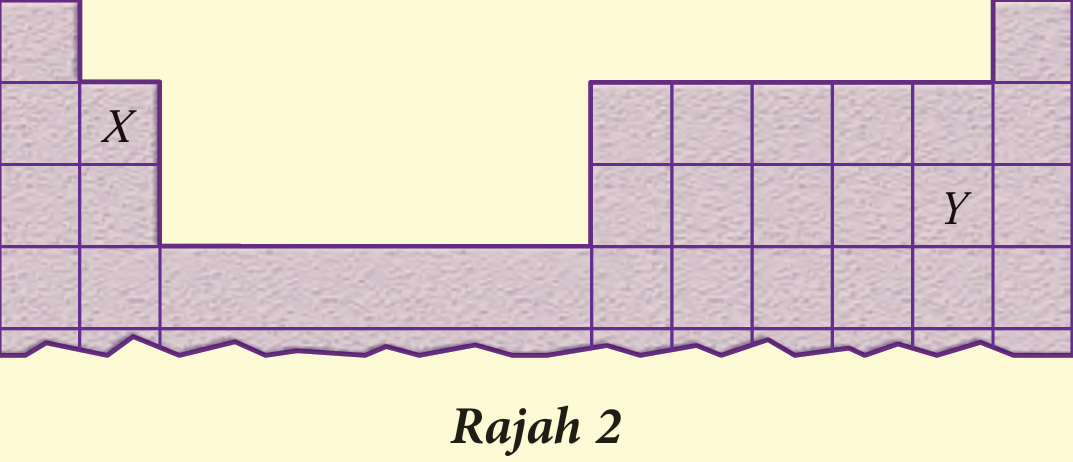
(a) Tulis susunan elektron bagi atom X dan Y.
(b) Jelaskan dua perbezaan sifat kimia antara unsur X dan Y.
(c) Mengapakah kereaktifan unsur-unsur yang sama kumpulan dengan X bertambah menuruni kumpulan, tetapi kereaktifan unsur-unsur yang sama kumpulan dengan Y berkurang?
Jawapan:
(a) Susunan elektron X = 2.2
Susunan elektron Y = 2.8.7
(b)

(c)
– Kereaktifan unsur yang sama kumpulan dengan Unsur X bergantung kepada kecenderungan atom melepaskan dua elektron
– Menuruni kumpulan, saiz atom bertambah menyebabkan jarak di antara nukleus dan elektron valens semakin jauh
– Daya tarikan nuklues terhadap elektron valens semakin lemah
– Atom lebih mudah melepaskan elektron. Oleh itu kereaktifan unsur bertambah menuruni kumpulan
– Kereaktifan unsur yang sama kumpulan dengan Unsur Y bergantung kepada kecenderungan atom menerima atau menarik satu elektron
– Menuruni kumpulan, saiz atom bertambah menyebabkan jarak di antara nukleus dan elektron semakin jauh
– Daya tarikan nukleus terhadap elektron semakin lemah
– Atom lebih sukar menerima atau menarik elektron. Oleh itu kereaktifan unsur berkurang menuruni kumpulan.
Rajah 2 menunjukkan beberapa unsur dalam Jadual Berkala Unsur yang diwakili dengan huruf X dan Y.

(a) Tulis susunan elektron bagi atom X dan Y.
(b) Jelaskan dua perbezaan sifat kimia antara unsur X dan Y.
(c) Mengapakah kereaktifan unsur-unsur yang sama kumpulan dengan X bertambah menuruni kumpulan, tetapi kereaktifan unsur-unsur yang sama kumpulan dengan Y berkurang?
Jawapan:
(a) Susunan elektron X = 2.2
Susunan elektron Y = 2.8.7
(b)

(c)
– Kereaktifan unsur yang sama kumpulan dengan Unsur X bergantung kepada kecenderungan atom melepaskan dua elektron
– Menuruni kumpulan, saiz atom bertambah menyebabkan jarak di antara nukleus dan elektron valens semakin jauh
– Daya tarikan nuklues terhadap elektron valens semakin lemah
– Atom lebih mudah melepaskan elektron. Oleh itu kereaktifan unsur bertambah menuruni kumpulan
– Kereaktifan unsur yang sama kumpulan dengan Unsur Y bergantung kepada kecenderungan atom menerima atau menarik satu elektron
– Menuruni kumpulan, saiz atom bertambah menyebabkan jarak di antara nukleus dan elektron semakin jauh
– Daya tarikan nukleus terhadap elektron semakin lemah
– Atom lebih sukar menerima atau menarik elektron. Oleh itu kereaktifan unsur berkurang menuruni kumpulan.
