Eksperimen 3A (Membandingkan Haba Peneutralan):
Tujuan: Menentukan dan membandingkan haba peneutralan antara asid dan alkali yang berlainan kekuatan.
A. Tindak balas asid kuat dengan alkali kuat dan asid lemah dengan alkali kuat
Penyataan masalah: Adakah tindak balas antara asid kuat dengan alkali kuat menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali kuat?
Hipotesis: Tindak balas antara asid kuat dengan alkali kuat menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali kuat.
Pemboleh ubah:
(a) Pemboleh ubah dimanipulasikan : Asid hidroklorik, HCl dan asid etanoik, CH3COOH.
(b) Pemboleh ubah bergerak balas : Haba peneutralan.
(c) Pemboleh ubah dimalarkan : Isi padu dan kepekatan larutan natrium hidroksida, NaOH.
Bahan: Asid hidroklorik, HCl 1.0 mol dm−3, asid etanoik, CH3COOH 1.0 mol dm−3 dan larutan natrium hidroksida, NaOH 1.0 mol dm−3.
Radas: Cawan polistirena dengan penutup, termometer dan silinder penyukat.
Prosedur:
1. Sukat dan tuang 50 cm3 asid hidroklorik, HCl 1.0 mol dm−3 ke dalam cawan polistirena.
2. Sukat dan tuang 50 cm3 larutan natrium hidroksida, NaOH 1.0 mol dm−3 ke dalam cawan polistirena yang lain.
3. Masukkan termometer ke dalam setiap larutan dan catatkan suhu awal setiap larutan.
4. Tuangkan asid hidroklorik, HCl 1.0 mol dm−3 dengan cepat dan cermat ke dalam larutan natrium hidroksida, NaOH 1.0 mol dm−3.
5. Kacau campuran dengan termometer.
6. Catatkan suhu tertinggi campuran.
7. Ulangi langkah 1 hingga 6 dengan menggantikan asid hidroklorik, HCl dengan asid etanoik, CH3COOH.
B. Tindak balas asid kuat dengan alkali lemah dan asid lemah dengan alkali lemah
Penyataan masalah: Adakah tindak balas antara asid kuat dengan alkali lemah menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali lemah?
Hipotesis: Bina satu hipotesis yang menghubungkan antara tindak balas asid kuat, asid lemah dengan alkali lemah dan haba peneutralan.
Pemboleh ubah: Nyatakan semua pemboleh ubah.
Bahan: Asid hidroklorik, HCl 1.0 mol dm−3, asid etanoik, CH3COOH 1.0 mol dm−3 dan larutan ammonia, NH3 1.0 mol dm−3.
Radas: Cawan polistirena dengan penutup, termometer dan silinder penyukat.
Prosedur:
Dengan menggunakan radas dan bahan yang dibekalkan, rancang dan jalankan eksperimen untuk menyiasat kesan kekuatan asid ke atas haba peneutralan dengan alkali lemah.
Keputusan:
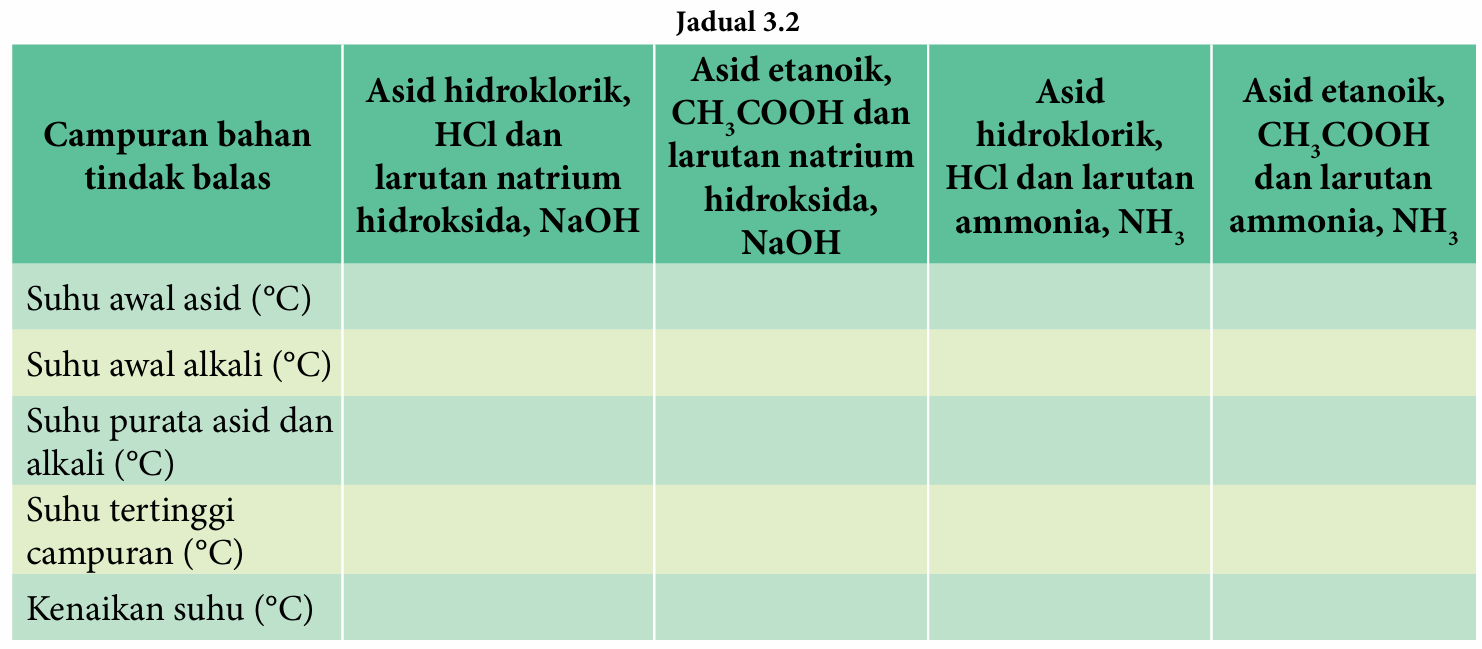
Salin dan lengkapkan Jadual 3.2 yang berikut untuk merekodkan suhu awal asid dan alkali, suhu purata asid dan alkali, suhu tertinggi dan kenaikan suhu.
Perbincangan:
1. Tuliskan persamaan kimia bagi setiap tindak balas peneutralan yang berlaku.
2. Hitungkan haba peneutralan, ∆H bagi setiap tindak balas.
[Muatan haba tentu larutan, c = 4.2 J g−1 °C−1; ketumpatan larutan = 1 g cm−3]
3. Lukiskan gambar rajah aras tenaga bagi setiap tindak balas peneutralan.
4. Bandingkan nilai haba peneutralan bagi setiap tindak balas peneutralan dalam eksperimen ini.
5. Terangkan sebab terdapat perbezaan dalam nilai haba peneutralan yang tersebut.
6. Nilai teori haba peneutralan antara asid kuat dan alkali kuat ialah -57 kJ mol−1. Bandingkan nilai ini dengan haba peneutralan yang telah anda peroleh dalam eksperimen ini. Nyatakan sebab bagi perbezaan ini.
Kesimpulan:
Adakah hipotesis dapat diterima? Apakah kesimpulan eksperimen ini?
Jawapan:
Hipotesis:
Tindak balas antara asid kuat dengan alkali lemah akan menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali lemah.
Perbincangan:
1.
$$ \begin{aligned} \mathrm{A}: & \mathrm{HCl}(\mathrm{ak})+\mathrm{NaOH}(\mathrm{ak}) \rightarrow \mathrm{NaCl}(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \\ & \mathrm{CH}_3 \mathrm{COOH}(\mathrm{ak})+\mathrm{NaOH}(\mathrm{ak}) \rightarrow \mathrm{CH}_3 \mathrm{COONa}(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \end{aligned} $$
$$ \begin{array}{ll} \mathrm{B}: & \mathrm{HCl}(\mathrm{ak})+\mathrm{NH}_3 \cdot \mathrm{H}_2 \mathrm{O}(\mathrm{ak}) \rightarrow \mathrm{NH}_4 \mathrm{Cl}(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \\ & \mathrm{CH}_3 \mathrm{COOH}(\mathrm{ak})+\mathrm{NH}_3 \cdot \mathrm{H}_2 \mathrm{O}(\mathrm{ak}) \rightarrow \mathrm{CH}_3 \mathrm{COONH}_4(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \end{array} $$
Nota: Penerangan tentang tindak balas peneutralan menggunakan ammonia akueus.
1. Persamaan kimia: HCl(ak) + NH3(ak) → NH4Cl(ak)
(Molekul NH4OH tidak wujud)
2. Peneutralan asid dengan alkali hasilkan garam dan air tetapi dalam kes ammonia akueus, air dalam persamaan tidak ditunjukkan.
3. Ammonia akueus, NH3 ialah satu alkali lemah yang mengalami pengionan separa untuk menghasilkan ion hidroksida, OH−.
NH3(ak) + H2O(ce) → NH4 + (ak) + OH−(ak)
4. Tindak balas peneutralan asid dengan ammonia akueus juga menghasilkan air dan ini dapat dilihat dalam persamaan ion.
5. Ion H+ daripada asid bertindak balas t dengan ion OH− daripada ammonia menghasilkan air.
Persamaan ion: H+(ak) + OH−(ak) → H2O(ce)
2. Daripada persamaan: 1 mol asid bertindak balas dengan 1 mol alkali.
Langkah-langkah penghitungan bagi setiap tindak balas:
(i) Hitungkan bilangan mol air yang terbentuk.
Bilangan mol ion H+ = bilangan mol asid
$$ =1.0 \mathrm{~mol} \mathrm{dm} \mathrm{~m}^{-3} \times \frac{50}{1000} \mathrm{dm}^3=0.05 \mathrm{~mol} \text { ion } \mathrm{H}^{+} $$
Bilangan mol ion OH− = bilangan mol alkali
$$ =1.0 \mathrm{~mol} \mathrm{dm} \mathrm{~m}^{-3} \times \frac{50}{1000} \mathrm{dm}^3=0.05 \mathrm{~mol} \text { ion } \mathrm{OH}^{-} $$
Maka, 0.05 mol ion H+ bertindak balas dengan 0.05 mol ion OH− untuk membentuk 0.05 mol air
(ii) Hitungkan perubahan haba:
Jumlah isi padu campuran = isi padu asid + isi padu alkali
= (50 cm3 + 50 cm3) = 100 cm3
Jisim campuran, m = 100 cm3 × 1 g cm3 = 100 g
Perubahan suhu larutan campuran, θ
Haba yang dibebaskan dalam tindak balas, Q = mcθ
= 100 g × 4.2 J g− oC−1 × θ = p J
(iii) Hitungkan haba peneutralan:
Peneutralan 0.05 mol ion H+ oleh 0.05 mol ion OH− membebaskan p J haba
Maka peneutralan 1 mol ion hidrogen oleh 1 mol ion hidroksida akan membebaskan
$$ p \mathrm{~J} \times \frac{1 \mathrm{~mol}}{0.05 \mathrm{~mol}}=q \mathrm{~J}=r \mathrm{~kJ} \mathrm{haba} $$
(iv) Tuliskan haba peneutralan bagi tindak balas antara asid dengan alkali ialah – r kJ mol−1
Nota: Letakkan tanda negatif kerana tindak balas peneutralan adalah eksotermik
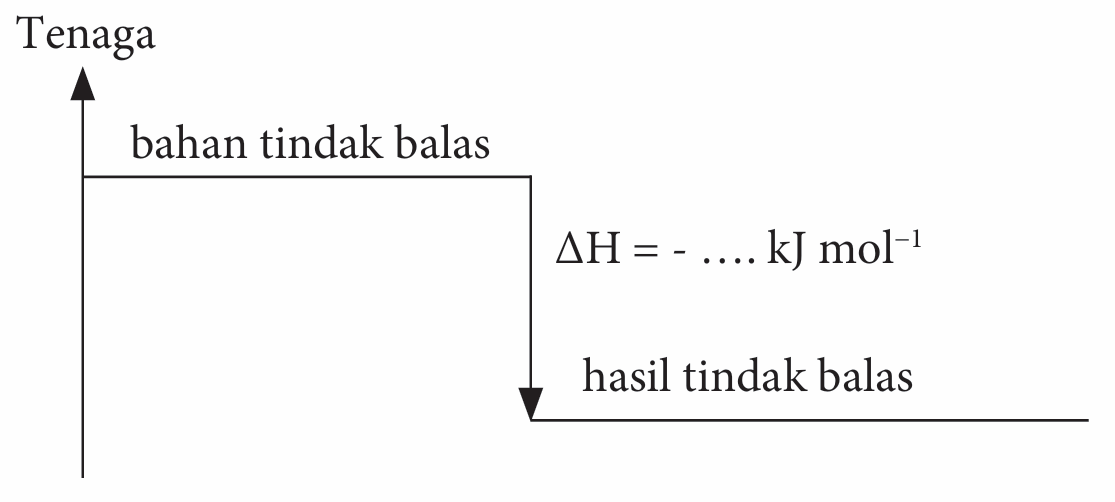
3. Lukiskan gambar rajah aras tenaga bagi setiap tindak balas seperti berikut:
Nota: Tuliskan formula untuk bahan tindak balas dan formula hasil tindak balas
4. Nilai haba peneutralan antara asid kuat dengan alkali kuat adalah lebih tinggi, daripada haba peneutralan menggunakan asid lemah dengan alkali kuat.
Nilai haba peneutralan antara asid kuat dengan alkali lemah lebih tinggi daripada haba peneutalan menggunakan asid lemah dengan alkali lemah.
Nilai haba peneutralan adalah paling tinggi bagi tindak balas antara asid kuat dengan alkali kuat.
Nilai haba peneutralan adalah paling rendah bagi tindak balas antara asid lemah dengan alkali lemah.
5. • Asid hidroklorik ialah asid kuat dan larutan natrium hidroksida ialah alkali kuat. Kedua-duanya mengion dengan lengkap dalam air untuk menghasilkan kepekatan ion yang tinggi.
• Tindak balas peneutralan hanya melibatkan gabungan ion hidrogen dan ion hidroksida untuk membentuk molekul air.
• Haba yang dibebaskan tidak perlu diserap semula untuk tujuan pengionan asid kuat atau alkali kuat
• Asid etanoik ialah asid lemah dan mengion separa lengkap dalam air. Kepekatan ion hidrogen adalah rendah kerana kebanyakan asid lemah wujud dalam bentuk molekul.
• Semasa peneutralan, sebahagian kecil haba yang dibebaskan semasa pembentukan 1 mol molekul air diserap semula oleh molekul asid etanoik untuk memecahkan ikatan O-H dalam molekul asid etanoik yang belum mengion.
• Apabila haba dibebaskan berkurang, maka haba peneutralan turut berkurang. Hal yang sama juga berlaku
kepada larutan ammonia akueus yang merupakan alkali lemah.
6. Nilai haba peneutralan yang diperolehi dalam eksperimen ini adalah lebih rendah. Ini disebabkan oleh:
(a) sebahagian haba terbebas ke persekitaran.
(b) cawan polistirena menyerap haba.
Tujuan: Menentukan dan membandingkan haba peneutralan antara asid dan alkali yang berlainan kekuatan.
A. Tindak balas asid kuat dengan alkali kuat dan asid lemah dengan alkali kuat
Penyataan masalah: Adakah tindak balas antara asid kuat dengan alkali kuat menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali kuat?
Hipotesis: Tindak balas antara asid kuat dengan alkali kuat menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali kuat.
Pemboleh ubah:
(a) Pemboleh ubah dimanipulasikan : Asid hidroklorik, HCl dan asid etanoik, CH3COOH.
(b) Pemboleh ubah bergerak balas : Haba peneutralan.
(c) Pemboleh ubah dimalarkan : Isi padu dan kepekatan larutan natrium hidroksida, NaOH.
Bahan: Asid hidroklorik, HCl 1.0 mol dm−3, asid etanoik, CH3COOH 1.0 mol dm−3 dan larutan natrium hidroksida, NaOH 1.0 mol dm−3.
Radas: Cawan polistirena dengan penutup, termometer dan silinder penyukat.
Prosedur:
1. Sukat dan tuang 50 cm3 asid hidroklorik, HCl 1.0 mol dm−3 ke dalam cawan polistirena.
2. Sukat dan tuang 50 cm3 larutan natrium hidroksida, NaOH 1.0 mol dm−3 ke dalam cawan polistirena yang lain.
3. Masukkan termometer ke dalam setiap larutan dan catatkan suhu awal setiap larutan.
4. Tuangkan asid hidroklorik, HCl 1.0 mol dm−3 dengan cepat dan cermat ke dalam larutan natrium hidroksida, NaOH 1.0 mol dm−3.
5. Kacau campuran dengan termometer.
6. Catatkan suhu tertinggi campuran.
7. Ulangi langkah 1 hingga 6 dengan menggantikan asid hidroklorik, HCl dengan asid etanoik, CH3COOH.
B. Tindak balas asid kuat dengan alkali lemah dan asid lemah dengan alkali lemah
Penyataan masalah: Adakah tindak balas antara asid kuat dengan alkali lemah menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali lemah?
Hipotesis: Bina satu hipotesis yang menghubungkan antara tindak balas asid kuat, asid lemah dengan alkali lemah dan haba peneutralan.
Pemboleh ubah: Nyatakan semua pemboleh ubah.
Bahan: Asid hidroklorik, HCl 1.0 mol dm−3, asid etanoik, CH3COOH 1.0 mol dm−3 dan larutan ammonia, NH3 1.0 mol dm−3.
Radas: Cawan polistirena dengan penutup, termometer dan silinder penyukat.
Prosedur:
Dengan menggunakan radas dan bahan yang dibekalkan, rancang dan jalankan eksperimen untuk menyiasat kesan kekuatan asid ke atas haba peneutralan dengan alkali lemah.
Keputusan:
Salin dan lengkapkan Jadual 3.2 yang berikut untuk merekodkan suhu awal asid dan alkali, suhu purata asid dan alkali, suhu tertinggi dan kenaikan suhu.

Perbincangan:
1. Tuliskan persamaan kimia bagi setiap tindak balas peneutralan yang berlaku.
2. Hitungkan haba peneutralan, ∆H bagi setiap tindak balas.
[Muatan haba tentu larutan, c = 4.2 J g−1 °C−1; ketumpatan larutan = 1 g cm−3]
3. Lukiskan gambar rajah aras tenaga bagi setiap tindak balas peneutralan.
4. Bandingkan nilai haba peneutralan bagi setiap tindak balas peneutralan dalam eksperimen ini.
5. Terangkan sebab terdapat perbezaan dalam nilai haba peneutralan yang tersebut.
6. Nilai teori haba peneutralan antara asid kuat dan alkali kuat ialah -57 kJ mol−1. Bandingkan nilai ini dengan haba peneutralan yang telah anda peroleh dalam eksperimen ini. Nyatakan sebab bagi perbezaan ini.
Kesimpulan:
Adakah hipotesis dapat diterima? Apakah kesimpulan eksperimen ini?
Jawapan:
Hipotesis:
Tindak balas antara asid kuat dengan alkali lemah akan menghasilkan haba peneutralan yang lebih tinggi daripada tindak balas asid lemah dengan alkali lemah.
Perbincangan:
1.
$$ \begin{aligned} \mathrm{A}: & \mathrm{HCl}(\mathrm{ak})+\mathrm{NaOH}(\mathrm{ak}) \rightarrow \mathrm{NaCl}(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \\ & \mathrm{CH}_3 \mathrm{COOH}(\mathrm{ak})+\mathrm{NaOH}(\mathrm{ak}) \rightarrow \mathrm{CH}_3 \mathrm{COONa}(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \end{aligned} $$
$$ \begin{array}{ll} \mathrm{B}: & \mathrm{HCl}(\mathrm{ak})+\mathrm{NH}_3 \cdot \mathrm{H}_2 \mathrm{O}(\mathrm{ak}) \rightarrow \mathrm{NH}_4 \mathrm{Cl}(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \\ & \mathrm{CH}_3 \mathrm{COOH}(\mathrm{ak})+\mathrm{NH}_3 \cdot \mathrm{H}_2 \mathrm{O}(\mathrm{ak}) \rightarrow \mathrm{CH}_3 \mathrm{COONH}_4(\mathrm{ak})+\mathrm{H}_2 \mathrm{O}(\mathrm{ce}) \end{array} $$
Nota: Penerangan tentang tindak balas peneutralan menggunakan ammonia akueus.
1. Persamaan kimia: HCl(ak) + NH3(ak) → NH4Cl(ak)
(Molekul NH4OH tidak wujud)
2. Peneutralan asid dengan alkali hasilkan garam dan air tetapi dalam kes ammonia akueus, air dalam persamaan tidak ditunjukkan.
3. Ammonia akueus, NH3 ialah satu alkali lemah yang mengalami pengionan separa untuk menghasilkan ion hidroksida, OH−.
NH3(ak) + H2O(ce) → NH4 + (ak) + OH−(ak)
4. Tindak balas peneutralan asid dengan ammonia akueus juga menghasilkan air dan ini dapat dilihat dalam persamaan ion.
5. Ion H+ daripada asid bertindak balas t dengan ion OH− daripada ammonia menghasilkan air.
Persamaan ion: H+(ak) + OH−(ak) → H2O(ce)
2. Daripada persamaan: 1 mol asid bertindak balas dengan 1 mol alkali.
Langkah-langkah penghitungan bagi setiap tindak balas:
(i) Hitungkan bilangan mol air yang terbentuk.
Bilangan mol ion H+ = bilangan mol asid
$$ =1.0 \mathrm{~mol} \mathrm{dm} \mathrm{~m}^{-3} \times \frac{50}{1000} \mathrm{dm}^3=0.05 \mathrm{~mol} \text { ion } \mathrm{H}^{+} $$
Bilangan mol ion OH− = bilangan mol alkali
$$ =1.0 \mathrm{~mol} \mathrm{dm} \mathrm{~m}^{-3} \times \frac{50}{1000} \mathrm{dm}^3=0.05 \mathrm{~mol} \text { ion } \mathrm{OH}^{-} $$
Maka, 0.05 mol ion H+ bertindak balas dengan 0.05 mol ion OH− untuk membentuk 0.05 mol air
(ii) Hitungkan perubahan haba:
Jumlah isi padu campuran = isi padu asid + isi padu alkali
= (50 cm3 + 50 cm3) = 100 cm3
Jisim campuran, m = 100 cm3 × 1 g cm3 = 100 g
Perubahan suhu larutan campuran, θ
Haba yang dibebaskan dalam tindak balas, Q = mcθ
= 100 g × 4.2 J g− oC−1 × θ = p J
(iii) Hitungkan haba peneutralan:
Peneutralan 0.05 mol ion H+ oleh 0.05 mol ion OH− membebaskan p J haba
Maka peneutralan 1 mol ion hidrogen oleh 1 mol ion hidroksida akan membebaskan
$$ p \mathrm{~J} \times \frac{1 \mathrm{~mol}}{0.05 \mathrm{~mol}}=q \mathrm{~J}=r \mathrm{~kJ} \mathrm{haba} $$
(iv) Tuliskan haba peneutralan bagi tindak balas antara asid dengan alkali ialah – r kJ mol−1
Nota: Letakkan tanda negatif kerana tindak balas peneutralan adalah eksotermik
3. Lukiskan gambar rajah aras tenaga bagi setiap tindak balas seperti berikut:
Nota: Tuliskan formula untuk bahan tindak balas dan formula hasil tindak balas

4. Nilai haba peneutralan antara asid kuat dengan alkali kuat adalah lebih tinggi, daripada haba peneutralan menggunakan asid lemah dengan alkali kuat.
Nilai haba peneutralan antara asid kuat dengan alkali lemah lebih tinggi daripada haba peneutalan menggunakan asid lemah dengan alkali lemah.
Nilai haba peneutralan adalah paling tinggi bagi tindak balas antara asid kuat dengan alkali kuat.
Nilai haba peneutralan adalah paling rendah bagi tindak balas antara asid lemah dengan alkali lemah.
5. • Asid hidroklorik ialah asid kuat dan larutan natrium hidroksida ialah alkali kuat. Kedua-duanya mengion dengan lengkap dalam air untuk menghasilkan kepekatan ion yang tinggi.
• Tindak balas peneutralan hanya melibatkan gabungan ion hidrogen dan ion hidroksida untuk membentuk molekul air.
• Haba yang dibebaskan tidak perlu diserap semula untuk tujuan pengionan asid kuat atau alkali kuat
• Asid etanoik ialah asid lemah dan mengion separa lengkap dalam air. Kepekatan ion hidrogen adalah rendah kerana kebanyakan asid lemah wujud dalam bentuk molekul.
• Semasa peneutralan, sebahagian kecil haba yang dibebaskan semasa pembentukan 1 mol molekul air diserap semula oleh molekul asid etanoik untuk memecahkan ikatan O-H dalam molekul asid etanoik yang belum mengion.
• Apabila haba dibebaskan berkurang, maka haba peneutralan turut berkurang. Hal yang sama juga berlaku
kepada larutan ammonia akueus yang merupakan alkali lemah.
6. Nilai haba peneutralan yang diperolehi dalam eksperimen ini adalah lebih rendah. Ini disebabkan oleh:
(a) sebahagian haba terbebas ke persekitaran.
(b) cawan polistirena menyerap haba.
