Eksperimen 4.2:
Tujuan: Mengkaji perubahan sifat kimia oksida unsur apabila merentasi Kala 3.
Pernyataan masalah: Bagaimanakah sifat kimia oksida unsur berubah apabila merentasi Kala 3?
Bahan: Natrium oksida, Na2O, magnesium oksida, MgO, aluminium oksida, Al2O3, gas sulfur dioksida, SO2, silikon(IV) oksida, SiO2, air suling, natrium hidroksida, NaOH 2.0 mol dm–3 dan asid nitrik, HNO3 2.0 mol dm–3
Radas: Tabung uji, penutup tabung uji, pemegang tabung uji, silinder penyukat 10 cm3, spatula, meter pH, penunu Bunsen dan rod kaca
(A) Tindak balas oksida unsur Kala 3 dengan air
Hipotesis: Merentasi Kala 3, oksida unsur berubah sifat daripada bes kepada asid.
Pemboleh ubah:
(a) dimanipulasikan : Jenis oksida unsur Kala 3
(b) bergerak balas : Perubahan dalam sifat oksida unsur
(c) dimalarkan : Isi padu air
Prosedur:
1. Tuangkan 10.0 cm3 air suling ke dalam tabung uji yang mengandungi separuh spatula natrium oksida, Na2O dan goncangkan.
2. Ukurkan nilai pH bagi larutan di dalam tabung uji itu dengan menggunakan meter pH.
3. Catatkan pemerhatian anda.
4. Ulang langkah 1 hingga 3 dengan menggunakan magnesium oksida, MgO, aluminium oksida, Al2O3 dan sulfur dioksida, SO2.
Keputusan:

(B) Tindak balas oksida unsur Kala 3 dengan natrium hidroksida dan asid nitrik
Buat hipotesis dan nyatakan semua pemboleh ubah bagi bahagian B.
Prosedur:
1. Masukkan 1/4 spatula serbuk magnesium oksida, MgO ke dalam dua tabung uji yang berasingan.
2. Tambahkan 5.0 cm3 natrium hidroksida, NaOH 2.0 mol dm–3 ke dalam tabung uji pertama.
3. Tambahkan 5.0 cm3 asid nitrik, HNO3 2.0 mol dm–3 ke dalam tabung uji kedua.
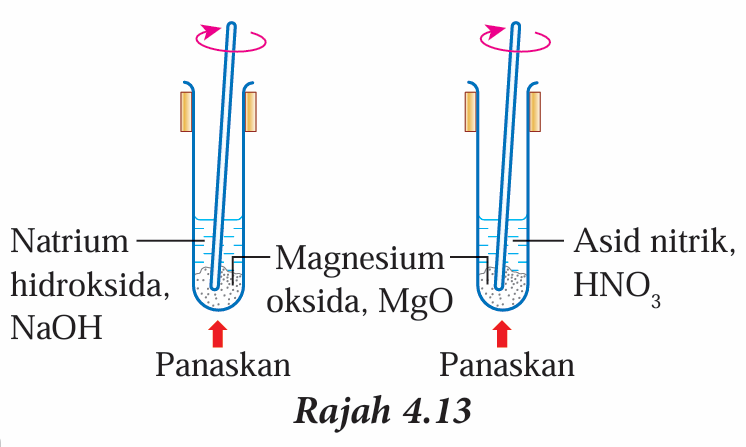
4. Panaskan kedua-dua tabung uji secara perlahan-lahan dan kacaukan dengan menggunakan rod kaca seperti yang ditunjukkan dalam Rajah 4.13.
5. Perhatikan keterlarutan oksida di dalam kedua-dua larutan dan catatkan pemerhatian anda.
6. Ulang langkah 1 hingga 5 dengan menggunakan aluminium oksida, Al2O3 dan silikon(IV) oksida, SiO2.
Keputusan:

Kesimpulan:
Adakah hipotesis yang dibuat dapat diterima? Apakah kesimpulan eksperimen ini?
Perbincangan:
1. Senaraikan oksida bes, oksida amfoterik dan oksida berasid.
2. Tulis persamaan kimia bagi tindak balas oksida bes dengan asid nitrik, HNO3.
3. Tulis persamaan kimia bagi tindak balas oksida amfoterik dengan natrium hidroksida, NaOH.
4. Senaraikan unsur yang mengandungi oksida bes dan oksida asid apabila merentasi Kala 3.
Jawapan:
Perbincangan
1. Oksida bes: Natrium oksida, Na2O, magnesium oksida (MgO)
Oksida amfoterik: Aluminium oksida (Al2O3)
Oksida berasid: Silikon(IV) oksida (SiO2), sulfur dioksida, SO2
2. MgO(p) + 2HNO3(ak) → Mg(NO3)2(ak) + H2O(ce)
3. Al2O3(p) + NaOH(ak) → NaAlO2(ak) + H2O(ce)
4. Unsur yang mengandungi oksida bes: Na dan Mg
Unsur yang mengandungi oksida asid: Si, P, S dan Cl
Tujuan: Mengkaji perubahan sifat kimia oksida unsur apabila merentasi Kala 3.
Pernyataan masalah: Bagaimanakah sifat kimia oksida unsur berubah apabila merentasi Kala 3?
Bahan: Natrium oksida, Na2O, magnesium oksida, MgO, aluminium oksida, Al2O3, gas sulfur dioksida, SO2, silikon(IV) oksida, SiO2, air suling, natrium hidroksida, NaOH 2.0 mol dm–3 dan asid nitrik, HNO3 2.0 mol dm–3
Radas: Tabung uji, penutup tabung uji, pemegang tabung uji, silinder penyukat 10 cm3, spatula, meter pH, penunu Bunsen dan rod kaca
(A) Tindak balas oksida unsur Kala 3 dengan air
Hipotesis: Merentasi Kala 3, oksida unsur berubah sifat daripada bes kepada asid.
Pemboleh ubah:
(a) dimanipulasikan : Jenis oksida unsur Kala 3
(b) bergerak balas : Perubahan dalam sifat oksida unsur
(c) dimalarkan : Isi padu air
Prosedur:
1. Tuangkan 10.0 cm3 air suling ke dalam tabung uji yang mengandungi separuh spatula natrium oksida, Na2O dan goncangkan.
2. Ukurkan nilai pH bagi larutan di dalam tabung uji itu dengan menggunakan meter pH.
3. Catatkan pemerhatian anda.
4. Ulang langkah 1 hingga 3 dengan menggunakan magnesium oksida, MgO, aluminium oksida, Al2O3 dan sulfur dioksida, SO2.
Keputusan:

(B) Tindak balas oksida unsur Kala 3 dengan natrium hidroksida dan asid nitrik
Buat hipotesis dan nyatakan semua pemboleh ubah bagi bahagian B.
Prosedur:
1. Masukkan 1/4 spatula serbuk magnesium oksida, MgO ke dalam dua tabung uji yang berasingan.
2. Tambahkan 5.0 cm3 natrium hidroksida, NaOH 2.0 mol dm–3 ke dalam tabung uji pertama.
3. Tambahkan 5.0 cm3 asid nitrik, HNO3 2.0 mol dm–3 ke dalam tabung uji kedua.
4. Panaskan kedua-dua tabung uji secara perlahan-lahan dan kacaukan dengan menggunakan rod kaca seperti yang ditunjukkan dalam Rajah 4.13.

5. Perhatikan keterlarutan oksida di dalam kedua-dua larutan dan catatkan pemerhatian anda.
6. Ulang langkah 1 hingga 5 dengan menggunakan aluminium oksida, Al2O3 dan silikon(IV) oksida, SiO2.
Keputusan:

Kesimpulan:
Adakah hipotesis yang dibuat dapat diterima? Apakah kesimpulan eksperimen ini?
Perbincangan:
1. Senaraikan oksida bes, oksida amfoterik dan oksida berasid.
2. Tulis persamaan kimia bagi tindak balas oksida bes dengan asid nitrik, HNO3.
3. Tulis persamaan kimia bagi tindak balas oksida amfoterik dengan natrium hidroksida, NaOH.
4. Senaraikan unsur yang mengandungi oksida bes dan oksida asid apabila merentasi Kala 3.
Jawapan:
Perbincangan
1. Oksida bes: Natrium oksida, Na2O, magnesium oksida (MgO)
Oksida amfoterik: Aluminium oksida (Al2O3)
Oksida berasid: Silikon(IV) oksida (SiO2), sulfur dioksida, SO2
2. MgO(p) + 2HNO3(ak) → Mg(NO3)2(ak) + H2O(ce)
3. Al2O3(p) + NaOH(ak) → NaAlO2(ak) + H2O(ce)
4. Unsur yang mengandungi oksida bes: Na dan Mg
Unsur yang mengandungi oksida asid: Si, P, S dan Cl
